
���� �ɳ�����ʯ�������������������������������������������������ݳ����������Ļ�ѧ����ʽ������ʽ���������������������
��� �⣺
��1�����ڷ�ӦFe2O3+3CO$\frac{\underline{\;����\;}}{\;}$2Fe+3CO2�У�CO��C�Ļ��ϼ���+2�ۣ����ߵ�CO2��+4�ۣ��Ǹû�ѧ��Ӧ�еĻ�ԭ����
��2���������Ͽ���������96%����������Ϊx��
Fe2O3+3CO$\frac{\underline{\;����\;}}{\;}$2Fe+3CO2
160 112
100t��80% 96%x
$\frac{160}{100t��80%}=\frac{112}{96%x}$
x=58t
�𰸣���1��CO����2����ұ��������96%������58t��
���� �����ѶȲ����麬�������ʵĻ�ѧ����ʽ�ļ��㣬ע����뷽��ʽ����ı����Ǵ����ʵ���������ȷ��������Ĺؼ���


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | Na2CO3��H2SO4��HCl��Ba��NO3��2 | B�� | NaOH��NaCl��HCl��FeCl3 | ||
| C�� | Na2SO4��BaCl2��HCl��K2CO3 | D�� | NaOH��NaCl��KNO3��MgCl2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
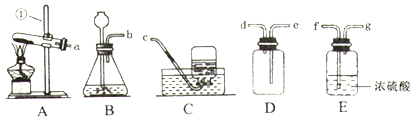
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
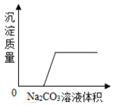 ij��ɫ��Һ��Ca��OH��2��HCl��H2SO4��NaCl��BaCl2�е�һ�ֻ�����ɣ������Һ�еμ�Na2CO3��Һ���������������������Na2CO3��Һ����Ĺ�ϵ��ͼ��ʾ������Һ��һ�����е������ǣ�д��ѧʽ����ͬ��HCl��BaCl2�����ܺ��е�������NaCl��
ij��ɫ��Һ��Ca��OH��2��HCl��H2SO4��NaCl��BaCl2�е�һ�ֻ�����ɣ������Һ�еμ�Na2CO3��Һ���������������������Na2CO3��Һ����Ĺ�ϵ��ͼ��ʾ������Һ��һ�����е������ǣ�д��ѧʽ����ͬ��HCl��BaCl2�����ܺ��е�������NaCl���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
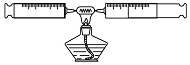 ��������ע������ɵ��ܱ�ϵͳ�ڹ���50mL����������ͼ��Ȼ���װ�к��IJ����ܼ��ȣ�ͬʱ�����ƶ�����ע�����Ļ��������������ڵĺ��ױ�ɰ��̣��ҽϳ�ʱ������һ���仯ʱֹͣ��ֹͣ���Ⱥ���ȴ�����½�����ȫ������һ��ע�����ڣ�
��������ע������ɵ��ܱ�ϵͳ�ڹ���50mL����������ͼ��Ȼ���װ�к��IJ����ܼ��ȣ�ͬʱ�����ƶ�����ע�����Ļ��������������ڵĺ��ױ�ɰ��̣��ҽϳ�ʱ������һ���仯ʱֹͣ��ֹͣ���Ⱥ���ȴ�����½�����ȫ������һ��ע�����ڣ��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ٶ� | B�� | �ڶ� | C�� | һ���� | D�� | ���ж� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com