
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:选择题
| A. | ①② | B. | ②③ | C. | ③④ | D. | ①②③④ |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
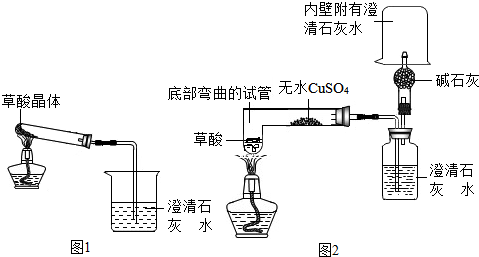
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 日本福岛核电站放射性碘在海啸时发生泄漏,碘这种元素被人们所认知.如图是元素周期表中提供的碘元素的部分信息及碘原子的结构示意图.
日本福岛核电站放射性碘在海啸时发生泄漏,碘这种元素被人们所认知.如图是元素周期表中提供的碘元素的部分信息及碘原子的结构示意图.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 紫色石蕊试液 | B. | pH试纸 | C. | 蓝色石蕊试液 | D. | 无色酚酞试液 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
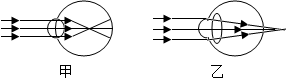 由于不良的学习习惯、上网游戏、偏食等因素的影响,青少年患近视的人数不断增加.请利用所学知识,完成以下与近视相关的部分探究活动.
由于不良的学习习惯、上网游戏、偏食等因素的影响,青少年患近视的人数不断增加.请利用所学知识,完成以下与近视相关的部分探究活动.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验操作 | 实验现象 | 实验结论 |
| ①取少量样品b于烧杯中,加足量蒸馏水,并用玻璃棒搅拌 | 样品全溶,形成无色溶液 | 猜想Ⅱ成立 |
| ②在①的溶液中加BaCl2溶液 | 无明显现象 | |
| ③在②得到的溶液中加少量AgNO3溶液 | 有白色沉淀生成,则添加的是MgCl2 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com