
·ÖĪö £Ø1£©øł¾Ż¼×ĶéČ¼ÉÕÉś³ÉĖ®ŗĶ¶žŃõ»ÆĢ¼Š“³ö»Æѧ·“Ó¦Ź½£»
£Ø2£©øł¾ŻĢģČ»ĘųŗĶŅŗ»ÆŹÆÓĶĘųµÄČ¼ÉÕŠčŅŖµÄŃõĘųæ¼ĀĒ£»
£Ø3£©“ÓĆŗµÄČ¼ÉÕ»įÉś³ÉĪŪČ¾æÕĘųµÄ¶žŃõ»ÆĮņæ¼ĀĒ£»
£Ø4£©æÉ“ÓČēŗĪ½ŚŌ¼ÓƵēµČ·½Ćęæ¼ĀĒ£»
½ā“š ½ā£ŗ
£Ø1£©ĢģČ»ĘųµÄÖ÷ŅŖ³É·ÖŹĒ¼×Ķ飬¼×ĶéČ¼ÉյĻÆѧ·½³ĢŹ½ĪŖ£ŗCH4+2O2$\frac{\underline{\;µćČ¼\;}}{\;}$CO2+2H2O
£Ø2£©±ūĶéČ¼ÉյĻÆѧ·½³ĢŹ½ĪŖ£ŗC3H8+5O2$\frac{\underline{\;µćČ¼\;}}{\;}$3CO2+4H2O
ÓɱūĶéŗĶ¼×ĶéČ¼ÉյĻÆѧ·½³ĢŹ½æÉÖŖ£¬Č¼ÉÕĻąĶ¬Ģå»żµÄ±ūĶéŗĶ¼×Ķ鏱£¬¼×ĶéŠčŅŖµÄŃõĘų½ĻÉŁ£®¹ŹĢī£ŗ±äŠ”£®
£Ø3£©ĢģČ»ĘųČ”“śĆŗµÄÓŵćŹĒ£ŗŌĖŹä»ņŹ¹ÓĆ·½±ć£¬»ņ²»»į²śÉś¶žŃõ»ÆĮņŌģ³ÉæÕĘųĪŪČ¾£®
£Ø4£©½ŚÄÜ»·±£ŹĒŅ»Ļī³¤ĘŚ¶ų¼č¾ŽµÄČĪĪń£¬ĪŅĆĒŅŖ³ä·ÖĄķ½ā£®¹ŹĢī£ŗ½ŚŌ¼ÓƵē£¬Ź¹ÓĆ½ŚÄܵēĘ÷µČ£®
“š°ø£ŗ
£Ø1£©¼×Ķé CH4+2O2$\frac{\underline{\;µćČ¼\;}}{\;}$CO2+2H2O
£Ø2£©±äŠ”
£Ø3£©²»»į²śÉś¶žŃõ»ÆĮņŌģ³ÉæÕĘųĪŪČ¾
£Ø4£©½ŚŌ¼ÓƵē£¬Ź¹ÓĆ½ŚÄܵēĘ÷µČ
µćĘĄ ±¾ĢāĶعż¶ŌŅŗ»ÆŹÆÓĶĘų”¢ĢģČ»ĘųČ¼ÉÕĻūŗĵÄŃõĘųµÄ±Č½Ļ£¬ĖµĆ÷ĮĖĢģČ»ĘųµÄÓÅŌ½ŠŌ£¬ŅŌ¼°æŖ·¢ŠĀÄÜŌ“µÄ±ŲŅŖŠŌ£®Ź¹»ÆѧÖŖŹ¶ČŚČėĮĖÉś»ī£®


 דŌŖ·»Č«³ĢĶ»Ęʵ¼Į·²āĻµĮŠ“š°ø
דŌŖ·»Č«³ĢĶ»Ęʵ¼Į·²āĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÓĆŅ»Ńõ»ÆĢ¼»¹ŌŃõ»ÆĶ£ŗCO+CuO$\frac{\underline{\;”÷\;}}{\;}$Cu+CO2£ØÖĆ»»·“Ó¦£© | |
| B£® | ĢśÓėŃĪĖį·“Ó¦£ŗ2Fe+6HClØT2FeCl3+3H2”ü£ØÖĆ»»·“Ó¦£© | |
| C£® | ŃĪĖįÓėĒāŃõ»ÆĶ·“Ó¦£ŗCu£ØOH£©2+2HClØTCuCl2+2H2O£Øø“·Ö½ā·“Ó¦£© | |
| D£® | ½«ĀČ»Æ±µČÜŅŗµĪČėĮņĖįĶČÜŅŗ£ŗCuSO4+BaCl2ØTBaSO4+CuCl2£Øø“·Ö½ā·“Ó¦£© |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
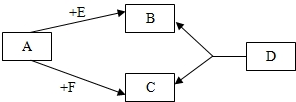 ŅŃÖŖA”¢E”¢FŹĒµ„ÖŹ£¬B”¢C”¢DŹĒ»ÆŗĻĪļ£¬¶¼ŹĒ³õÖŠ³£¼ūµÄĪļÖŹ£¬ĖüĆĒ·Ö±šŹĒÓÉĢ¼”¢Ēā”¢ŃõČżÖÖŌŖĖŲÖŠµÄŅ»ÖÖ»ņÕß¼øÖÖ×é³É£®ĘäÖŠBŹĒĻą¶Ō·Ö×ÓÖŹĮæ×īŠ”µÄŃõ»ÆĪļ£¬DĪļÖŹŗܲ»ĪČ¶Ø£¬ČŻŅ×·Ö½āÉś³ÉBŗĶC£¬ĖüĆĒÖ®¼äµÄ×Ŗ»Æ¹ŲĻµČēĶ¼ĖłŹ¾£®
ŅŃÖŖA”¢E”¢FŹĒµ„ÖŹ£¬B”¢C”¢DŹĒ»ÆŗĻĪļ£¬¶¼ŹĒ³õÖŠ³£¼ūµÄĪļÖŹ£¬ĖüĆĒ·Ö±šŹĒÓÉĢ¼”¢Ēā”¢ŃõČżÖÖŌŖĖŲÖŠµÄŅ»ÖÖ»ņÕß¼øÖÖ×é³É£®ĘäÖŠBŹĒĻą¶Ō·Ö×ÓÖŹĮæ×īŠ”µÄŃõ»ÆĪļ£¬DĪļÖŹŗܲ»ĪČ¶Ø£¬ČŻŅ×·Ö½āÉś³ÉBŗĶC£¬ĖüĆĒÖ®¼äµÄ×Ŗ»Æ¹ŲĻµČēĶ¼ĖłŹ¾£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÓĆČ¼×ŵÄľĢõ¼ų±šŃõĘųŗĶ¶žŃõ»ÆĢ¼ | B£® | ÓĆĻõĖįŅųČÜŅŗ¼ų±šĻ”ŃĪĖįŗĶŹ³ŃĪĖ® | ||
| C£® | ÓĆĖ®¼ų±šĢ¼ĖįøĘ·ŪÄ©ŗĶĢ¼ĖįÄĘ·ŪÄ© | D£® | ÓĆ×ĘÉյķ½·Ø¼ų±šĆŽ²¼ŗĶĖæ³ń |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® | 112£ŗ27£ŗ28 | B£® | 336£ŗ27£ŗ56 | C£® | 28£ŗ81£ŗ7 | D£® | 56£ŗ81£ŗ112 |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com