
| 23-A | 23-B |
| 硅胶是无色或白色颗粒,可反复使用,其主要成分是SiO2. ①SiO2中Si元素的化合价为+4. ②SiO2中Si元素的质量分数约为46.7%,其计算式为$\frac{28}{28+16×2}×100%$. | 铁粉常用于食品保鲜. ①铁粉用于食品保鲜的原因是铁与空气中反应生成了氢氧化铁的缘故. ②写出上述反应的化学方程式4Fe+6H2O+3O2=4Fe(OH)3. |
分析 (1)根据人体所需六大营养素的种类、食物来源,结合题中所给的食物判断所含的营养素,进行分析判断.
(2)23-A根据在化合物中正负化合价代数和为零,结合SiO2的化学式进行解答本题.根据化合物中元素质量分数的计算方法来分析.
23-B根据铁与氧气、水反应生成氢氧化铁进行分析解答.
解答 解:(1)酸奶、酱牛肉要富含蛋白质;面条中富含糖类;果汁中富含维生素,故填:酸奶、酱牛肉.
(2)23-A,在二氧化硅中,氧元素显-2价,设硅元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:x+(-2)×2=0,则x=+4价.
二氧化硅中硅元素的质量分数为:$\frac{28}{28+16×2}$×100%≈46.7%.
23-B,铁与氧气、水反应生成氢氧化铁,其反应的化学方程式为:4Fe+6H2O+3O2=4Fe(OH)3.
故答案为:
| 23-A | 23-B |
| ①+4 ②$\frac{28}{28+16×2}$×100% | ②4Fe+6H2O+3O2=4Fe(OH)3 |
点评 本题难度不大,掌握利用化合价的原则计算指定元素的化合价的方法、化学式的计算以及化学方程式的书写方法等即可正确解答本题.


科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 木炭在氧气中燃烧:发出白光 | B. | 硫粉在氧气中燃烧:淡蓝色火焰 | ||
| C. | 白磷在空气中燃烧:白色烟雾 | D. | 铁丝在空气中燃烧:火星四射 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
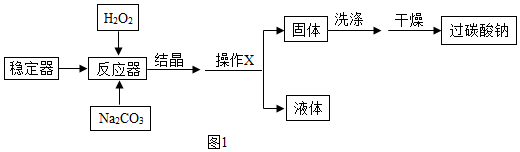
 小明同学新买了一台氧立得便携式制氧器,其中有A、B两包固体,B包为黑色固体粉未,经查阅资料知A包主要成分为过碳酸钠.将A包、B包药品分别放入机器,就可以制得氧气.为探究A包固体的纯度,设计了如图2所示实验装置.
小明同学新买了一台氧立得便携式制氧器,其中有A、B两包固体,B包为黑色固体粉未,经查阅资料知A包主要成分为过碳酸钠.将A包、B包药品分别放入机器,就可以制得氧气.为探究A包固体的纯度,设计了如图2所示实验装置.查看答案和解析>>
科目:初中化学 来源: 题型:计算题
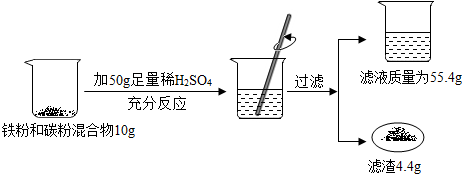
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 44% | B. | 66% | C. | 32% | D. | 68% |
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| 选项 | A | B | C | D |
| 实验设计 | 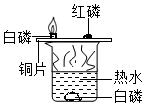 |  |  | 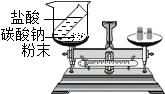 |
| 实验目的 | 探究燃烧条件之一:空气 | 探究水的组成 | 探究铁、铜的金属活动强弱 | 探究化学发应是否遵循质量守恒定律 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | KOH和FeCl3 | B. | MgCO3和HCl | C. | Na2CO3和CaCl2 | D. | Ba(OH)2和K2SO4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com