
铝跟稀H2SO4反应生成氢气和硫酸铝(铝是+3价),下列化学方程式中,正确的是
A.Al+H2SO4![]() AlSO4+H2↑
AlSO4+H2↑
B.2Al+3H2SO4![]() Al(SO4)3+H2
Al(SO4)3+H2
C.2Al+3H2SO4![]() Al2(SO4)3+3H2↑
Al2(SO4)3+3H2↑
D.3Al+H2SO4![]() Al2SO4+H2↑
Al2SO4+H2↑
科目:初中化学 来源: 题型:阅读理解
| 酸及反应进程 | 1min | 2min | 5min | 15min | 20min |
| a% HCl | 少量气泡 | 较多气泡 | 大量气泡 | 反应剧烈 | 铝片耗尽 |
| b% H2SO4 | 均无明显现象(无气泡) | ||||
| c% H2SO4 | 均无明显现象(无气泡) | ||||
查看答案和解析>>
科目:初中化学 来源: 题型:
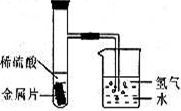 Ⅰ某自然科学兴趣小组设计了如下图所示的装置,用来研究不同金属跟稀硫酸反应的快慢.他们用此装置,选择了甲、乙、丙、丁四种大小相同的金属片,分别与相同体积、相同溶质质量分数的稀硫酸反应,观察在30s里从导管口冒出的氢气泡多少,记录在下表中.(“+”越多表示产生的气泡越多)
Ⅰ某自然科学兴趣小组设计了如下图所示的装置,用来研究不同金属跟稀硫酸反应的快慢.他们用此装置,选择了甲、乙、丙、丁四种大小相同的金属片,分别与相同体积、相同溶质质量分数的稀硫酸反应,观察在30s里从导管口冒出的氢气泡多少,记录在下表中.(“+”越多表示产生的气泡越多)| 金属 | 甲 | 乙 | 丙 | 丁 |
| 氢气泡的多少 | ++ | ++++ | +++ | + |
| 实验步骤 | 实验现象 |
| ①在试管里取少量盐酸,插入铁丝,充分作用 | 溶液由无色变为浅绿色,有大量气体生成 |
| ②在①所得的溶液中,插入 铜丝 铜丝 ,充分作用 |
无明显现象 |
| ③在②所得溶液中,插入 铝丝 铝丝 ,充分作用 |
金属铝表面有一层,黑色物质生成 |
查看答案和解析>>
科目:初中化学 来源:题网九年级上化学鲁教版 鲁教版 题型:013
铝跟稀H2SO4反应生成氢气和硫酸铝(铝是+3价),下列化学方程式中,正确的是
A.Al+H2SO4![]() AlSO4+H2↑
AlSO4+H2↑
B.2Al+3H2SO4![]() Al(SO4)3+H2
Al(SO4)3+H2
C.2Al+3H2SO4![]() Al2(SO4)3+3H2↑
Al2(SO4)3+3H2↑
D.3Al+H2SO4![]() Al2SO4+H2↑
Al2SO4+H2↑
查看答案和解析>>
科目:初中化学 来源:不详 题型:问答题
| 酸及反应进程 | 1min | 2min | 5min | 15min | 20min |
| a% HCl | 少量气泡 | 较多气泡 | 大量气泡 | 反应剧烈 | 铝片耗尽 |
| b% H2SO4 | 均无明显现象(无气泡) | ||||
| c% H2SO4 | 均无明显现象(无气泡) | ||||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com