
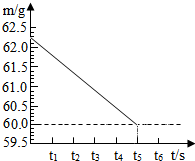
 将碳酸钠和硫酸钠的固体混合物6g放入烧杯中(烧杯质量为20g),再加入36.2g稀硫酸,在一定时间内恰好完全反应,无固体剩余.反应时间(t)和烧杯及其所盛物质的总质量(m)的关系如图所示:
将碳酸钠和硫酸钠的固体混合物6g放入烧杯中(烧杯质量为20g),再加入36.2g稀硫酸,在一定时间内恰好完全反应,无固体剩余.反应时间(t)和烧杯及其所盛物质的总质量(m)的关系如图所示:分析 (1)根据碳酸钠与硫酸反应会生成二氧化碳,硫酸钠不反应,所以反应前后装置减少的质量为二氧化碳的质量进行分析;
根据二氧化碳的质量结合碳酸钠和稀硫酸反应的化学方程式可以求算出碳酸钠的质量,进而求算出碳酸钠的质量分数;
(2)利用(1)中所求碳酸钠的质量,进一步可得到原混合物中硫酸钠的质量,再利用该反应可求生成的硫酸钠的质量,然后利用溶液中溶质的质量分数进行计算即可.
解答 解:(1)二氧化碳的质量=62.2g-60.0g=2.2g;
(2)设原有碳酸钠的质量为x,生成硫酸钠的质量为y,
Na2CO3+H2SO4═Na2SO4+H2O+CO2↑
106 142 44
x y 2.2g
$\frac{106}{x}$=$\frac{142}{y}$=$\frac{44}{2.2g}$
x=5.3g
y=7.1g
6g固体混合物中硫酸钠的质量是6g-5.3g=0.7g;
(3)所得溶液中溶质质量分数为:$\frac{6g-5.3g+7.1g}{6g+36.2g-2.2g}$×100%=19.5%.
故答案为:(1)2.2,0.7;
(2)19.5%.
点评 本考点既考查了根据化学方程式的计算,又考查了溶质的质量分数和质量守恒定律,属于含杂质的计算,综合性比较强,属于图象型计算题,是中考计算题中经常出现的题型.做题时要注意:化学方程式要写正确,杂质是否溶于水、是否反应等问题.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:选择题
| A. | 它是一种化合物 | |
| B. | 其中氧元素与氢元素的质量比为8:1 | |
| C. | 其中碳元素的质量分数为50% | |
| D. | 一个丙烯酸分子由3个碳原子、4个氢原子和1个氧分子构成 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | H2S SO2 H2SO4 | B. | SO2 S H2SO3 | ||
| C. | SO3 H2S SO2 | D. | S SO2 H2S |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 20℃时100克氯化钠溶液中含有36克氯化钠 | |
| B. | 20℃时100克氯化钠饱和溶液中含有36克氯化钠 | |
| C. | 20℃时100克水中达到饱和状态时能溶解36克氯化钠 | |
| D. | 20℃时氯化钠溶液中溶质的质量分数为36% |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
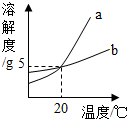 如图是a、b两种固体物质(不含结晶水)的溶解度曲线.下列说法正确的是( )
如图是a、b两种固体物质(不含结晶水)的溶解度曲线.下列说法正确的是( )| A. | b的溶解度大于a的溶解度 | |
| B. | 20℃时,将a、b两种物质的饱和溶液分别恒温蒸发等质量的水,析出晶体的质量一定相等 | |
| C. | 将20℃时的b的不饱和溶液降温,一定能得到b的饱和溶 液 | |
| D. | 当温度高于20℃时,a溶液的溶质质量分数一定大于b溶液的溶质质量分数 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
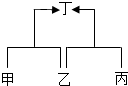 已知甲、乙、丙、丁是初中化学中的四种常见物质,丁是甲与乙、乙与丙反应的生成物之一(反应条件均已略去),转化关系如图:
已知甲、乙、丙、丁是初中化学中的四种常见物质,丁是甲与乙、乙与丙反应的生成物之一(反应条件均已略去),转化关系如图:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com