
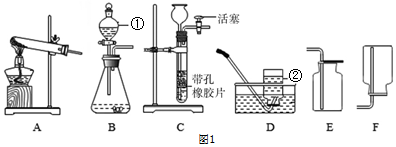
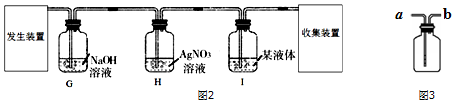
分析 (1)根据实验室常用仪器解答;
(2)根据实验室用双氧水制取氧气的原理写出反应的方程式,根据装置特点分析解答;
(3)实验室制取气体时选择药品产生气体速度适中,便于收集,药品要廉价易得等,据此进行分析解答;
(4)根据实验室制取甲烷气体的反应所使用药品及反应条件,判断所应选用的发生装置,并根据甲烷的溶解性与密度,判断收集甲烷应选用的收集装置;
(5)根据物质的性质进行分析,盐酸具有挥发性解答;
①根据硝酸银溶液能检验氯化氢气体的存在解答;
②根据浓硫酸具有吸水性解答.
解答 解:
(1)根据实验室常用仪器可知:②是集气瓶;
(2)实验室用双氧水制取氧气,发生反应的化学方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.仪器 ①的作用是:便于添加液体药品、控制滴加液体速率可以控制化学反应的速率;
(3)实验室中用大理石和稀盐酸反应制取二氧化碳,主要是因为二者反应速率适中,容易控制,并且药品价格合理等.
石灰石与稀盐酸反应制取二氧化碳,同时生成氯化钙、水,反应的化学方程式是:CaCO3+2HCl=CaCl2+H2O+CO2↑.
在反应过程中,使反应停止的操作是:关闭活塞,使液体和固体分离;
(4)实验室常用加热醋酸钠和碱石灰的固体混合物来制取甲烷(CH4)气体,故应先用装置A作为反应的发生装置,由于甲烷是一种无色无味、密度比空气小、极难溶于水的气体,故可采取装置D向下排空气法或装置E;甲烷的密度比空气小,若用图3装置收集甲烷,气体应从b端导入;
(5)盐酸具有挥发性,用锌粒和稀盐酸制取氢气,小华认为小明制取的氢气不纯,杂质气体除了水蒸气外还含有氯化氢;
①氯化氢溶于水形成盐酸,盐酸能与硝酸银溶液反应生成白色氯化银沉淀,所以H中硝酸银溶液的作用是:检验氯化氢已除尽(或证明氯化氢已除尽);
②氢氧化钠溶液能和氯化氢反应,从而除去氯化氢,浓硫酸能吸收水蒸气,从而干燥气体,故I中液体是浓硫酸.
答案:
(1)集气瓶;
(2)2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑; 便于添加液体药品、控制滴加液体速率可以控制化学反应的速率(合理即可);
(3)CaCO3+2HCl═CaCl2+CO2↑+H2O; 关闭活塞;
(4)AF或AD; b;
(5)HCl;
①检验氯化氢已除尽(或证明氯化氢已除尽); ②浓硫酸.
点评 本题难度不大,是中考的重要考点之一,熟练掌握实验室中制取气体的反应原理、发生装置和收集装置的选择依据是正确解答本题的关键.


科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | 物质 | 方法 |
| A | NaCl(CaCl2) | 加入适量Na2CO3溶液,过滤、洗涤、干燥 |
| B | N2 (O2) | 通入灼热的铜网 |
| C | NaOH溶液(Ca(OH)2) | 加入过量碳酸钠溶液,充分反应后过滤 |
| D | CaO粉末(CaCO3) | 加入适量稀盐酸,充分搅拌后过滤 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
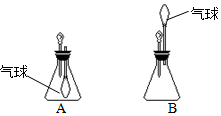
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
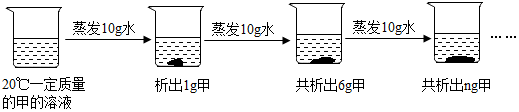
| A. | 蒸发前原溶液是饱和溶液 | |
| B. | n的数值是12 | |
| C. | 甲物质在20℃时的溶解度是50g | |
| D. | 甲物质的溶解度随温度的升高而增大 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 2016年12月26日,合肥地铁一号线正式通车,实现了我省地下交通的新突破.根据如图回答下列问题:
2016年12月26日,合肥地铁一号线正式通车,实现了我省地下交通的新突破.根据如图回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
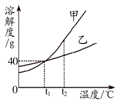
| A. | t1℃时,甲溶液中溶质的质量分数一定等于乙溶液 | |
| B. | 降低温度,可使甲的饱和溶液变为不饱和溶液 | |
| C. | t2℃时,分别在100 g水中加入50 g 甲、乙,同时降温至t1℃,甲、乙溶液均为饱和溶液 | |
| D. | 将t2℃时甲的饱和溶液降温至t1℃,溶液质量不变 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com