
【题目】2020年新型冠状病毒引起的肺炎在我国部分地区造成的疫情在全国人民的共同努力下得到了较好的控制。为防传染,很多部门用过氧乙酸对环境消毒,已知过氧乙酸的化学式为C2H4O3。下列有关过氧乙酸的说法正确的是()
A.属于无机物
B.氧元素质量分数最大
C.相对分子质量为78
D.是由2个碳原子、4个氢原子和3个氧原子构成
 同步练习强化拓展系列答案
同步练习强化拓展系列答案科目:初中化学 来源: 题型:
【题目】(8分)竖炉冶铁工艺流程如图8所示。
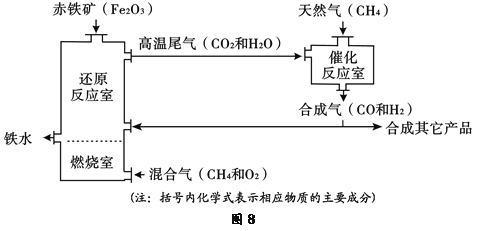
回答下列问题:
(1)该工艺流程中,甲烷的作用是 ,冶炼出的铁水属于 (填“纯净物”或“混合物”)。
(2)用化学方程式表示还原反应室内炼铁的原理 。(写一个)
(3)该工艺流程中,可循环利用的物质是 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】人类在生产、生活中离不开能源。
(1)从环境保护的角度考虑,下列燃料最理想的是_______(填字母)。
A汽油
B一氧化碳
C甲烷
D氢气
(2)下列各混合物遇明火可能会发生爆炸的是_______(填字母)。
A氢气和氧气
B一氧化碳和甲烷
C面粉弥散在空气中
D二氧化碳和氧气
(3)自热盒饭用到一种白色氧化物——生石灰,该氧化物遇水会放出大量的热,达到加热饭菜的目的。试写出该反应的化学方程式_______。
(4)下列成语主要体现“提供可燃物”这一原理的是________(填字母)。
A扇风点火
B火上浇油
C钻木取火
D釜底抽薪
(5)已知某可燃物1.6g在空气中充分燃烧,生成4.4g二氧化碳和3.6g水,则下列说法不正确的是________(填字母)。
A该可燃物中碳、氢元素质量比为1:4
B可燃物中氢元素的质量分数为25%
C该可燃物一定不含氧元素
D生成二氧化碳和水的分子个数比为1:2
(6)焊接或切割金属常用乙炔(C2H2)做燃料,试写出其在空气中充分燃烧的化学方程式_______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】氧气是生产生活中重要的物质.
如图是水厂利用水库中的水生产自来水的主要流程:
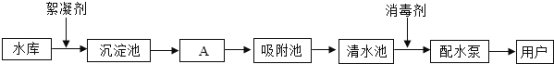
(1)水库中的水属于________(填“纯净物”或“混合物”);
(2)二氧化氯(ClO2)是一种高效的消毒剂,其中氯元素的化合价为_____;
(3)我国规定水质必须在一定感官性指标、化学指标、病理学指标等方面达标后才能成为饮用水。
感官性指标:水应澄清透明,未达到此要求可加入明矾使杂质沉降,通过____________(填操作名称)而实现;
化学指标:包括水的pH和硬度两项,然后生活中区分硬水和软水最简便的方法是用___________区分;
病理学指标对细菌的含量有严格的限制,可以通过__________操作,既能杀菌又能得到几乎纯净的水;
(4)请举出水在实验中的一种用途___________;
(5)加入絮凝剂的目的是______________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图是教材中有关《质量守恒定律》的实验,试回答下列问题:
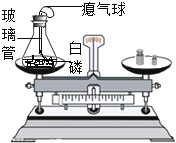
(1)反应中锥形瓶内观察到的现象是______;
(2)左盘锥形瓶口在白磷点燃后要塞紧瓶塞,原因是______;
(3)在实验设计上,玻璃管上方系一瘪气球的目的是______;
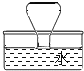
(4)实验结束后(锥形瓶已冷却到室温),发现瓶中白磷过量,为了防止白磷在空气中燃烧,将锥形瓶瓶口倒置于盛满水的水槽中(如图,瓶口贴紧水面),拔下瓶塞,发现水进入锥形瓶中,则进入瓶中的水占锥形瓶的容积的1/5,原因是:______.
某化学课外小组同学,用如图所示实验验证质量守恒定律。
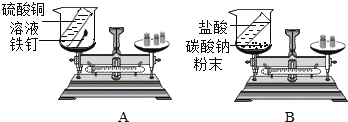
(5)某甲同学用A装置探究质量守恒定律,实验步骤如下:如图将烧杯放在天平上用砝码平衡,然后倾斜烧杯使硫酸铜溶液与铁钉接触,一段时间后,再把烧杯放在天平上。
①烧杯内反应的实验现象为___
②最后天平的指针(填序号)___(a 偏左b 偏右c 不偏转d 无法预测).
(6)①乙同学用B装置研究质量守恒定律,实验步骤如下:
将烧杯放在天平上用砝码平衡,然后倾斜烧杯使盐酸与碳酸钠粉末接触,写出反应的化学方程式___;一段时间后再把烧杯放在天平上,发现天平的指针偏右,该反应___(填符合或不符合)质量守恒定律。
②若在验证质量守恒定律时,若利用有气体参加或有气体生成的化学反应来设计实验,在装置设计方面应做到___.
③从微观角度解释化学反应都符合质量守恒定律___.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某实验小组选择“铜和硫酸反应的探究”的课题开展探究,下表是他们分别用相同质量的铜粉和足量硫酸反应的几组实验数据:
实验编号 | 硫酸的质量分数/% | 温度/℃ | 铜粉消失的时间/s |
① | 98 | 120 | 400 |
② | 98 | 200 | 200 |
③ | 80 | 120 | 500 |
④ | 80 | 200 | 280 |
⑤ | 70 | 200 | 不消失 |
⑥ | 40 | 200 | 不消失 |
(1)实验①、②表明:该反应快慢与__________有关,其关系是_______________;能表明硫酸浓度对反应快慢有影响的实验编号组合是_____________。
(2)如果把实验①中硫酸的质量分数改为85%,请你推出铜粉消失时间(用t表示)的取值范围_______。
(3)从上表来看,能与铜粉发生反应的硫酸溶液最低浓度a%的范围是_________(取整数)。
(4)影响金属和酸化学反应速度的因素除了上述因素以外还可能有____________________。
(拓展延伸)已知浓硫酸与铜粉加热时产生刺激性气体氧化物,同时溶液变蓝。如图是利用压强传感器测定浓硫酸与铜粉加热产生气体与NaOH溶液产生喷泉实验过程及压强变化曲线图。
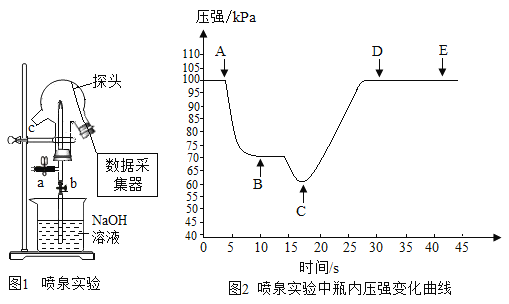
(5)请写出铜粉与浓硫酸加热生成刺激性气体和溶液变蓝的化学方程式_________________。
(6)实验过程:三颈瓶内装有收集满的气体,采集数据,将吸有NaOH溶液的胶头滴管塞紧颈口c,挤尽胶头滴管液体,然后打开阀门b,烧杯内的NaOH溶液喷到三颈瓶内形成喷泉,则曲线AB段下降的原因是_____________;CD段上升的原因是___________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】以下实验均是初中化学课本上的实验,请回答有关问题。
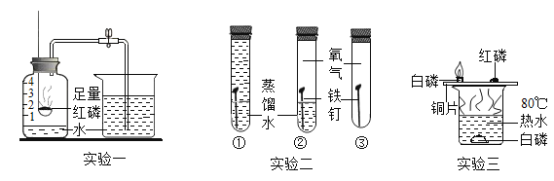
(1)实验一的目的是_____;
(2)实验二中,一段时间后,试管_____ 里的铁钉生锈;
(3)实验三中铜片上的白磷燃烧而红磷不燃烧,这一现象说明燃烧的条件之一是_______;
(4)上述实验中, 需要通过对比分析得出实验结论的是_______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】盐场晒盐后得到的卤水中含有MgCl2、KCl和MgSO4等物质,它们的溶解度曲线如图所示。下列说法正确的是
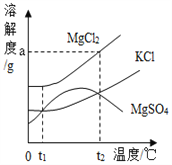
A. MgSO4的溶解度始终随温度的升高而减小
B. t1℃时,KCl和MgSO4两溶液所含溶质的质量一定相等
C. t2℃时,100g MgCl2的饱和溶液中含有ag MgCl2
D. 将t2℃时的MgSO4饱和溶液降温到t1℃,溶液的变化是:饱和→不饱和→饱和
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】请从1或2两题中任选1个作答。
O2的实验室制取与性质 | CO2的实验室制取与性质 |
(1)A中加热高锰酸钾,发生反应的化学方程式为___________。 (2)B中可观察到的现象是__________。 |
(1)A中向大理石中加入稀盐酸,发生反应的化学方程式为__________。 (2)B中可观察到的现象是__________。 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com