
 小鹏与小明做完酸、碱、盐相关性质实验后,很感兴趣地把稀硫酸、氢氧化钠溶液和碳酸钠溶液混合一起,看到有大量气泡生成.他们对反应后溶液中溶质的成分很好奇,请你与他们一起进行研究.
小鹏与小明做完酸、碱、盐相关性质实验后,很感兴趣地把稀硫酸、氢氧化钠溶液和碳酸钠溶液混合一起,看到有大量气泡生成.他们对反应后溶液中溶质的成分很好奇,请你与他们一起进行研究.| 第一次 | 第二次 | 第三次 | 第四次 | 第五次 | |
| 加入纯碱样品的质量/g | 5.4 | 5.4 | 5.4 | 5.4 | 5.4 |
| 电子天平的示数/g | 163.2 | 166.4 | 169.6 | 175 | 180.4 |
分析 【猜想假设】根据碳酸钠和硫酸能反应,不能共存解答;
【实验探究】(1)根据硫酸钠溶液和硫酸溶液,不能使无色酚酞变色解答;
(2)根据稀硫酸的溶液显酸性,能和氧化铜反应,溶液变蓝,说明溶液中有硫酸并写出化学方程式;
【实验结论】根据碳酸钠的溶液显碱性,稀硫酸的溶液显酸性,滴加无色酚酞,发现溶液颜色无变化,排除①②,向盛有少量氧化铜粉末的试管中加入适量该溶液,振荡,溶液变蓝,排除⑤;
【拓展应用】根据酸与碱发生中和反应解答;
(1)根据质量守恒定律,由反应前后烧杯及所盛物质总质量的差,计算生成二氧化碳的质量;
(2)根据完全反应后所放出二氧化碳的质量,计算样品中碳酸钠的质量,由碳酸钠质量与样品质量比计算样品中碳酸钠质量分数进行解答;
(3)根据完全反应后所放出二氧化碳的质量,计算所用稀盐酸的质量即可进行解答.
解答 解:【猜想假设】稀硫酸、氢氧化钠溶液和碳酸钠溶液混合一起反应时,如果稀硫酸滴加过快,稀硫酸和碳酸钠反应,开始也会产生气泡,有二氧化碳生成,有可能没把氢氧化钠消耗完,稀硫酸已经没有了,故①合理;碳酸钠和硫酸能反应,不能共存,故④不合理;
【实验探究】(1)取少量该溶液于试管中,向其中滴加无色酚酞,发现溶液颜色无变化,说明溶液中无碳酸钠和氢氧化钠,故②③都符合,因此小鹏的结论是不合理,理由是②Na2SO4、H2SO4也不能使无色酚酞变色;
(2)向盛有少量氧化铜粉末的试管中加入适量该溶液,振荡,溶液变蓝.说明溶液中有硫酸,化学方程式为:CuO+H2SO4═CuSO4+H2O;
【实验结论】碳酸钠的溶液显碱性,稀硫酸的溶液显酸性,滴加无色酚酞,发现溶液颜色无变化,排除①⑤;向盛有少量氧化铜粉末的试管中加入适量该溶液,振荡,溶液变蓝,说明了溶液中含有硫酸,排除③.所以猜想②是正确的;
【拓展应用】实验室的酸性废水必须处理至中性再排放可以减少水的污染;
(1)根据质量守恒定律,第一次加入纯碱样品充分反应后,生成二氧化碳的质量=100g+60g+5.4g-163.2g=2.2g;
(2)第三次加入纯碱样品充分反应后与100g盐酸恰好完全反应,共生成二氧化碳的质量为:5.4g×3+100g+60g-169.6g=6.6g
设前三次样品中含有碳酸钠的质量为x,所用稀盐酸中溶质的质量为y.
Na2CO3+2HCl═2NaCl+H2O+CO2↑
106 73 44
x y 6.6g
$\frac{106}{x}$=$\frac{73}{y}$=$\frac{44}{6.6g}$
x=15.9g
y=10.95g
纯碱样品中碳酸钠的质量分数=$\frac{15.9g}{5.4g×3}$×100%≈98.1%;
(3)所用稀盐酸的质量分数=$\frac{10.95g}{100g}$×100%=10.95%.
故答案为:【猜想假设】④;
【实验探究】(1)不合理,②Na2SO4、H2SO4也不能使无色酚酞变色;
(2)CuO+H2SO4═CuSO4+H2O;
【实验结论】②;
【拓展应用】减少水的污染;
(1)第一次加入纯碱样品充分反应后,生成二氧化碳的质量是2.2g;
(2)纯碱样品中碳酸钠的质量分数约为98.1%;
(3)所用稀盐酸的质量分数是10.95%.
点评 本题主要考查化学实验方案的设计与评价,根据物质的性质和物质间的反应规律,学会运用猜想与事实验证的方法和技巧处理实验问题和利用化学方程式进行计算的能力.


 中考解读考点精练系列答案
中考解读考点精练系列答案科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 ”表示氧原子,“
”表示氧原子,“ ”表示氢原子.请回答下列问题.
”表示氢原子.请回答下列问题.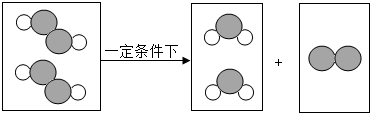
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
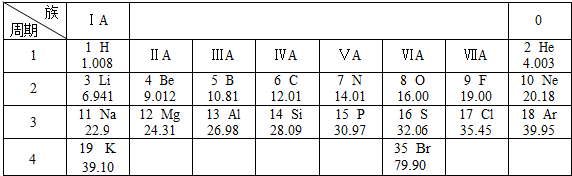
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 多食水果和蔬菜,给人体补充维生素 | |
| B. | 汽车使用乙醇汽油,减少有害气体的排放 | |
| C. | 用肥皂水涂抹蚊子叮咬处,可以减轻痛痒 | |
| D. | 用甲醛溶液浸泡水产品,防止水产品腐败变质 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 红磷在空气中燃烧产生大量白烟 | |
| B. | 镁在空气中燃烧,发出耀眼的白光,生成白色固体 | |
| C. | 铁丝在氧气中剧烈燃烧,火星四射,生成黑色固体 | |
| D. | 硫在氧气中燃烧产生淡蓝色火焰,生成有刺激性气味的气体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com