
| 实验次序 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| H2O2溶液溶质质量分数 | 1% | 3% | 5% | 10% | 15% | 20% | 25% | 30% |
| MnO2粉末用量(g) | 0.2 | 0.2 | 0.2 | 0.2 | 0.2 | 0.2 | 0.2 | 0.2 |
| 收集一瓶气体时所用时间(秒) | 660 | 220 | 205 | 80 | 25 | 9 | 4 | 3 |
| 反应后液体温度(℃) | 24 | 34 | 39 | 56 | 65 | 67 | 69 | 70 |
| 实验次序 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| MnO2粉末用量(g) | 0.1 | 0.2 | 0.3 | 0.4 | 0.5 | 0.6 | 0.7 | 0.8 | 0.9 | 1.0 |
| 所用时间(秒) | 17 | 8 | 7 | 5 | 4 | 3 | 2 | 2 | 2 | 2 |
分析 (1)根据对根据质量守恒定律正确书写化学方程式或文字表达式,
(2)根据收集时的观察要求分析.
(3)根据观察过氧化氢溶液浓度越大,收集气体用的时间多少和溶液温度的高低考虑.
(4)根据表格中收集一瓶气体所需时间可知是否受影响;从“反应后液体温度”可知是放热反应;
(5)图表中数据的分析考虑;
(6)在常温下很难分解得到氧气,其分解速度受浓度、温度、催化剂等因素的影响设计实验方案来证明时,要注意实验的控制变量,以确保实验结果的准确性.
解答 解:(1)用双氧水和二氧化锰制氧气的反应物是过氧化氢,生成物是水和氧气,反应条件是二氧化锰作催化剂,用观察法配平,氧气后面标上上升符号;
故填:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑(或过氧化氢$\stackrel{二氧化锰}{→}$水+氧气);
(2)为准确测定收集一瓶气体所需的时间,实验时宜采用排水方法来收集氧气;因为易于观察是否恰好收集满.故填:排水;
(3)由图表中数据可知H2O2溶液的溶质质量分数越大,收集到一瓶气体时所用时间越短,即反应速度越快;故填:双氧水浓度越大,其分解的速率越快;
(4)随着反应的进行,溶液温度越来越高,所以该反应是放热反应;故填:放热;
(5)根据图表中数据可知,当催化剂MnO2的用量增加时,收集氧气时所用的时间越来越短,即反应速度越来越快;增加到0.7g后反应速度不再改变了;故填:MnO2对H2O2的分解起催化作用,且MnO2达到一定量时,它的多少不改变反应速率;
(6)影响过氧化氢分解速率的因素还有催化剂的种类.可以取浓度相同、质量相同的过氧化氢溶液分别加入不同种类的同质量的催化剂进行实验,测定收集一瓶氧气所需的时间即可.故答案为:催化剂种类;取浓度相同、质量相同的过氧化氢溶液分别加入不同种类的同质量的催化剂进行实验,测定收集一瓶氧气所需的时间即可.
点评 解答本题关键是要知道方程式的书写方法,知道反应速度的影响因素有:温度,反应物浓度,反应物的接触面积,知道根据图示数据分析问题的方法.


 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案 名校名师培优作业本加核心试卷系列答案
名校名师培优作业本加核心试卷系列答案科目:初中化学 来源: 题型:选择题
| A. | 硫+氧气$\stackrel{点燃}{→}$ 二氧化硫 | B. | 石蜡+氧气$\stackrel{点燃}{→}$二氧化碳+水 | ||
| C. | 红磷+氧气$\stackrel{点燃}{→}$ 五氧化二磷 | D. | 镁+氧气$\stackrel{点燃}{→}$氧化镁 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 组别 | 待鉴别物质 | 鉴别试剂或方法一 | 鉴别试剂或方法二 |
| A | 淀粉溶液、鸡蛋清溶液 | 碘水 | 硫酸铜溶液 |
| B | 食盐水、硫酸钾溶液 | BaCl2溶液 | AgNO3溶液 |
| C | 食盐水、苏打水 | 盐酸 | 酚酞试液 |
| D | 高度白酒、白醋 | NaHCO3溶液 | 点燃 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
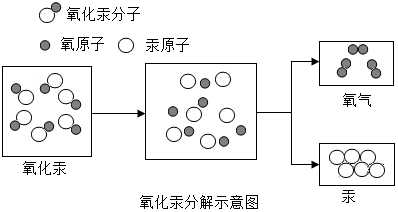
| A. | 氧化汞受热时分解为汞和氧气 | |
| B. | 在化学变化中分子可以再分,而原子不能再分 | |
| C. | 所有的物质都是由分子构成的 | |
| D. | 保持汞的化学性质的最小粒子是汞原子,保持氧化汞的化学性质的最小粒子是氧化汞分子 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
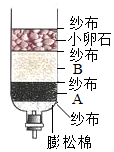 2013年春我国北方出现大面积干旱.在一些偏远山区饮水问题异常困难.小冬从出后的水塘中取来一桶浑浊的水,利用化学上学到净水原理,制作了简易的净水器,如图所示,使用时,水从上端加入,从下端流出.
2013年春我国北方出现大面积干旱.在一些偏远山区饮水问题异常困难.小冬从出后的水塘中取来一桶浑浊的水,利用化学上学到净水原理,制作了简易的净水器,如图所示,使用时,水从上端加入,从下端流出.查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com