
| A. | -2价 | B. | -4价 | C. | +4价 | D. | +6价 |
 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:计算题
 “垃圾放错地方的资源”,实验室也要环保.实验室用稀盐酸和大理石制取CO2,取50g反应后的滤液,逐滴滴入碳酸钠溶液,测得滴入碳酸钠溶液的质量与产生沉淀质量的关系曲线如图所示.回答下列问题:
“垃圾放错地方的资源”,实验室也要环保.实验室用稀盐酸和大理石制取CO2,取50g反应后的滤液,逐滴滴入碳酸钠溶液,测得滴入碳酸钠溶液的质量与产生沉淀质量的关系曲线如图所示.回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:计算题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题

| A. | ①② | B. | ①⑤ | C. | ③④ | D. | ①②⑤ |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. |  | B. | 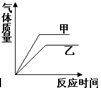 | C. |  | D. | 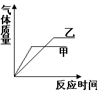 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
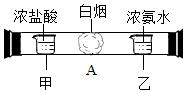 某同学想探究“气体分子的运动快慢与气体的相对分子质量的关系”.他提出了下列假设:相对分子质量越大,分子运动速率越小.于是,他设计并做了以下实验:在甲、乙两烧杯中分别盛放浓盐酸和浓氨水(能挥发出氨气NH3),把它们分别同时放在一两端开口的玻璃管两端,然后塞紧橡皮塞(如图).观察到玻璃管A处出现白烟(白烟是氯化氢气体与氨气反应生成的氯化铵固体).
某同学想探究“气体分子的运动快慢与气体的相对分子质量的关系”.他提出了下列假设:相对分子质量越大,分子运动速率越小.于是,他设计并做了以下实验:在甲、乙两烧杯中分别盛放浓盐酸和浓氨水(能挥发出氨气NH3),把它们分别同时放在一两端开口的玻璃管两端,然后塞紧橡皮塞(如图).观察到玻璃管A处出现白烟(白烟是氯化氢气体与氨气反应生成的氯化铵固体).查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com