(1)NH4Cl 在10℃时溶解度为33g,则10℃时NH4Cl 饱和溶液的溶质质量分数为______,200g饱和溶液含NH4Cl______g,含水______g.
(2)把一定质量的30%的某溶液加热蒸发10g水,冷却至20℃时,有2g晶体析出,此时溶液的质量分数为40%,则该物质在20℃时的溶解度为______g.
解:(1)NH
4Cl在10℃时溶解度为33g,则10℃时NH
4Cl饱和溶液的溶质质量分数为
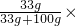
100%≈24.8%.
200g该温度下的饱和溶液含NH
4Cl的质量为200g×24.8%=49.6g,含水的质量为200g-49.6g=150.4g.
(2)把一定质量的30%的某溶液加热蒸发10g水,冷却至20℃时,有2g晶体析出,所得溶液为20℃时的饱和溶液,饱和溶液中溶质的质量分数为40%,
设该物质在20℃时的溶解度为S,则

100%=40%,S=66.7g
故答案为:(1)24.8%;49.6g;150.4g;(2)66.7.
分析:(1)根据饱和溶液的溶质质量分数=

100%,进溶质质量=溶液质量×溶质的质量分数,溶剂质量=溶液质量-溶质质量即可求得水的质量,据此进行分析解答.
(2)将原溶液蒸发掉10g水后,冷却至20℃析出了晶体,根据饱和溶液的定义可知,该溶液为20℃时的饱和溶液,此时的溶质的质量分数即为该温度下的饱和溶液的质量分数,据此可计算出20℃时该物质的溶解度.
点评:本题难度不大,掌握饱和溶液的溶质质量分数的计算方法、溶质质量分数的有关计算等是正确解答本题的关键.

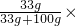 100%≈24.8%.
100%≈24.8%. 100%=40%,S=66.7g
100%=40%,S=66.7g 100%,进溶质质量=溶液质量×溶质的质量分数,溶剂质量=溶液质量-溶质质量即可求得水的质量,据此进行分析解答.
100%,进溶质质量=溶液质量×溶质的质量分数,溶剂质量=溶液质量-溶质质量即可求得水的质量,据此进行分析解答.

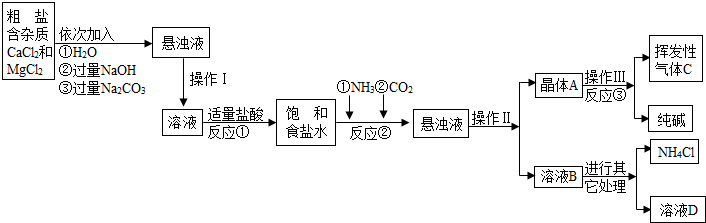



 (2013?平江区二模)请写出下列相关的化学反应方程式并完成题后填空:
(2013?平江区二模)请写出下列相关的化学反应方程式并完成题后填空: