
分析 I.(1)根据铝和氧化铁在高温的条件下生成铁和氧化铝,以及化合价原则求出元素的化合价;
(2)根据一氧化碳和氧化铁在高温的条件下生成铁和二氧化碳,二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水进行分析;
II.(1)根据锌和稀硫酸反应生成硫酸锌和氢气进行分析;
(2)根据氧化铜和稀硫酸反应生成硫酸铜和水,氧化锌和稀硫酸反应生成硫酸锌和水,加入的稀硫酸是过量的进行分析;
(3)根据分离混合物的方法以及过滤和蒸发操作中需要的仪器进行分析;
(4)根据反应的化学方程式进行分析.
解答 解:I.(1)铝和氧化铁在高温的条件下生成铁和氧化铝,化学方程式为:Fe2O3+2Al$\frac{\underline{\;高温\;}}{\;}$Al2O3+2Fe,在氧化铁中铁元素的化合价为+3价,在铁中元素的化合价为0价,所以此过程中铁元素的化合价由+3价变为0价;
(2)一氧化碳和氧化铁在高温的条件下生成铁和二氧化碳,化学方程式为:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2,二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水,化学方程式为:CO2+Ca(OH)2=CaCO3↓+H2O;
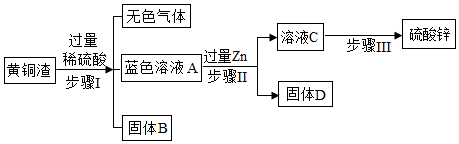
II.(1)锌和稀硫酸反应生成硫酸锌和氢气,化学方程式为:Zn+H2SO4=ZnSO4+H2↑;
(2)氧化铜和稀硫酸反应生成硫酸铜和水,氧化锌和稀硫酸反应生成硫酸锌和水,加入的稀硫酸是过量的,所以溶液A中的溶质有:ZnSO4、CuSO4、H2SO4;
(3)由图可知,操作Ⅰ过滤除去铜和杂质,操作Ⅱ过滤是除去锌和置换出的铜,此操作要用到的玻璃仪器有玻璃棒、烧杯和漏斗;
(4)A到C的过程中发生的反应是:Zn+CuSO4=Cu+ZnSO4,
160 161
由此可见,锌置换出了溶液中的铜,溶液的质量增重了.
故答案为:I.(1)Fe2O3+2Al$\frac{\underline{\;高温\;}}{\;}$Al2O3+2Fe,+3,0;
(2)Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2,CO2+Ca(OH)2=CaCO3↓+H2O;
II.(1)Zn+H2SO4=ZnSO4+H2↑;
(2)ZnSO4、CuSO4、H2SO4;
(3)过滤,漏斗;
(4)大于.
点评 本题重点考查了金属活动性顺序及其应用,了解相关知识即可正确解答.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:选择题
| A. | 水是由2个氢原子和1个氧原子构成 | B. | 冰变成水,水分子之间间隙变大了 | ||
| C. | 水中氢原子和氧原子个数比为2:1 | D. | 质子数相同的粒子属于同种元素 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
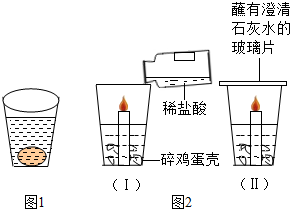 生活中处处有化学,小明把学到的化学知识用于生活中,进行下列探究.
生活中处处有化学,小明把学到的化学知识用于生活中,进行下列探究.查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
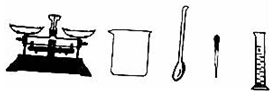
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
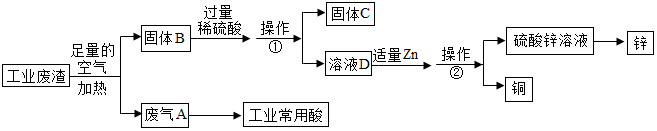
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
| 次数 | 第1次 | 第2次 | 第3次 | 第4次 |
| 烧杯内混合物质量/g | 149.6 | 199.2 | 249.0 | 299.0 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com