
4.6g常见的有机物A在空气中完全燃烧,产生二氧化碳8.8g,产生水蒸气5.4g
有机物A的名称____________________
若有机物A不完全燃烧,只产生一氧化碳和水,请问此4.6g有机物A不完全燃烧最多能产生多少克有毒气体?
 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:计算题
H7N9型禽流感病毒近期在国内华东地区蔓延,引起人们的恐慌与担忧.治疗禽流感的特效药帕拉米韦氯化钠注射液,临床证明其对H7N9型的禽流感病毒有明确疗效.帕拉米韦的化学式为CxH28N4O4,相对分子质量为328.请计算:
(1)帕拉米韦的化学式(CxH28N4O4)中x= ;
(2)帕拉米韦中氧元素的质量分数为 (精确到0.1%)
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
新型材料纳米级Fe粉具有广泛的用途,它比普通Fe粉更易与氧气反应,其制备工艺流程如下图所示: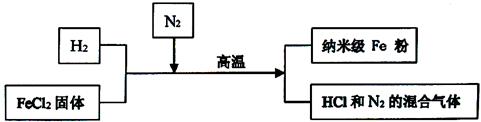
请回答下列问题:
(1)纳米级Fe粉在氧气中能自发燃烧生成黑色固体,此黑色固体的化学式为 。
(2)请补充完成上述制备工艺的化学方程式:H2 +FeCl2  Fe+ 。
Fe+ 。
(3)研究人员发现最后制得的纳米级Fe粉样品中混有少量的FeCl2杂质。
①为除去样品中的杂质,在无氧环境下,先加 溶解,然后再 、洗涤、烘干.
②取样品20g,加入足量的盐酸,生成氢气0.7g。请计算该样品中单质Fe的质量分数。
(请写出计算过程)____ 。
查看答案和解析>>
科目:初中化学 来源: 题型:探究题
过碳酸钠(Na2CO4)在洗涤、印染、纺织、造纸、医药卫生等领域有大量应用,某化学研究性学习小组设计并完成了如下实验。
【实验目的】测定过碳酸钠样品(含有的杂质不溶于水且不与酸反应)的纯度。
【实验原理】2Na2CO4+ 4HCl → 4NaCl + 2CO2↑+ O2↑+ 2H2O
【实验装置】
【交流与讨论】
①甲同学认为测定产物中O2的体积即可测定样品的纯度。装置②的作用是:(15);装置③的作用是:(16);
②乙同学认为测定产物中CO2的质量(即反应前后装置②的质量差)就可测定样品的纯度。但利用上述实验装置测得CO2的质量并计算样品的纯度,结果会偏高,你认为原因可能是;(17)(填序号)
A.浓盐酸易挥发,产生的氯化氢气体被装置②吸收
B.二氧化碳气体逸出时带出的水蒸气在装置②中冷凝而被吸收
C.装置①、②内空气中的二氧化碳被装置②吸收
③丙同学提出了一种新方案,得到了大家的一致认可:称取样品12.5g,滴加足量浓盐酸至样品反应完全,再将烧瓶中所有的液体蒸发、结晶、烘干,得到0.2mol氯化钠。则该样品的中过碳酸钠的质量分数为多少?(写出计算过程)
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
科学小组的同学对模拟湿法炼铜实验中得到的
铁、铜固体混合物进行含量测定。称取10克
固体混合物置于烧杯中,滴加一定质量分数的
稀硫酸溶液,记录并绘制了如图所示的曲线。
(1)10克固体混合物中铜的质量为______克。
(2)所用稀硫酸溶液溶质的质量分数是多少?(写出计算过程)
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
某同学在实验室发现一瓶由碳酸钠和氯化钠组成的混合溶液.为了测定该混合溶液中碳酸钠的质量分数,该同学设计了如下实验:取该混合溶液50g,向其中逐滴加入稀盐酸,当加入盐酸的质量为15g、30g、45g、60g时,生成气体的质量见下表(气体的溶解度忽略不计).
| | 第Ⅰ组 | 第Ⅱ组 | 第Ⅲ组 | 第Ⅳ组 |
| 稀盐酸的质量/g | 15 | 30 | 45 | 60 |
| 生成气体的质量/g | 1.8 | n | 4.4 | 4.4 |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
某同学做了如下图所示的实验,在14.6%的稀盐酸中加入碳酸钙,后加入10.6%的碳酸钠溶液
| | 第一次 | 第二次 |
| 14.6%的稀盐酸的质量 | m | m |
| 加入碳酸钙的质量 | 10g | 20g |
| 加入10.6%的碳酸钠溶液的质量 | 100g | 200g |
| 加入碳酸钠溶液后,实验现象 | 只有气泡 | 只有白色沉淀 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com