
【题目】如图为初中化学实验室制取气体的常用装置,请回答有关问题:

(1)写出仪器a的主要用途:______。
(2)实验室用高锰酸钾制取并收集氧气时,应选择的实验装置是______,若用装置C收集的氧气不纯,原因可能是_____;用过氧化氢溶液和二氧化锰制取氧气时,选用B装置可得到平稳的氧气气流,其操作方法是______。
(3)利用B装置可制取的气体有H2、O2和_____等,请写出实验室制取所填气体的化学方程式:_____;若用F装置干燥该气体,气体应从______(填“b”或“c”)端通入。
【答案】作为少量试剂的反应容器 AC(或AD) 导管口刚冒出气泡就开始收集 将过氧化氢溶液通过注射器缓慢均匀地滴入锥形瓶中 CO2 CaCO3+2HCl-CaCl2+H2O+CO2↑ b
【解析】
(1)通过分析题中所指仪器的作用可知,a是试管,主要用途是:作为少量试剂的反应容器;
(2)实验室用高锰酸钾制取氧气的反应物是固体,反应条件是加热,氧气的密度比空气大,不易溶于水,所以实验室用高锰酸钾制取并收集氧气时,应选择的实验装置是AC或AD,用排水法收集氧气,不纯的原因是:收集时刻过早或集气瓶没有装满水,注射器可以控制液体的滴加速度,所以用过氧化氢溶液和二氧化锰制取氧气时,选用B装置可得到平稳的氧气气流,其操作方法是:将过氧化氢溶液通过注射器缓慢均匀的滴入锥形瓶中;
(3)B装置制取气体的反应物是固体和液体,反应条件是常温,所以利用B装置可制取的气体有H2、O2和CO2等,碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑,洗气时,应该长进短出,所以用F装置干燥该气体,气体应从b端通入。


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
【题目】阅读下面科普短文。
新冠疫情以来,全球出现了“口罩荒”,其中熔喷布更是成为制约口罩产能增长的关键因素。
“熔喷布”俗称口罩的“心脏”,是生产医用外科口罩与N95口罩的重要原料。熔喷布由于使用易加工、性能好、耐药性能优异的聚丙烯 (C3H6)n作为原料,所以空隙率更高,比表面积更多、过滤效率更好、绝缘性能也十分优异。口罩合不合格很大程度上取决于熔喷布是否合格,质量检测是熔喷布从采购、生产、销售到使用的重要环节。
检测一 熔喷布的内在质量指标应符合图1
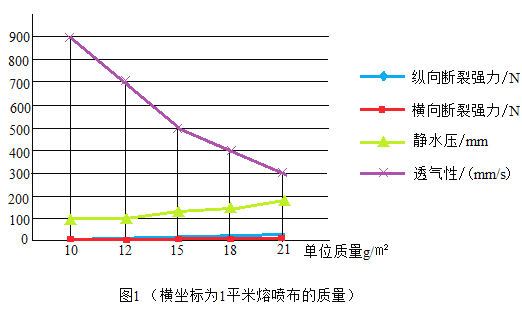
检测二熔喷布的微生物指标应符合表1
表1 产品微生物指标要求
项目 | 要求 |
细菌菌落总数/(CFU/g) ≤ | 200 |
真菌菌落总数/(CFU/g) ≤ | 100 |
大肠菌群 | 不得检出 |
致病性化脓菌 | 不得检出 |
检测三 熔喷布外观质量应符合表2的要求
表2 外观质量要求
项目 | 要求 |
布面外观 | 均匀、平整、无明显折痕和死折:产品应该干燥、清洁、无污染 |
面积大于4mm2的孔 | 不允许 |
昆虫、灰尘和金属粉末等非正常物质 | 不允许 |
异常气味 | 不允许 |
卫生和医疗用品的微孔和晶点 | 不允许 |
熔喷布作为医疗卫生用布,主要用来制造医用防护服、手术衣、医用口罩、尿片、消毒包布、卫生巾等产品。
依据文章内容回答下列问题。
(1)聚丙烯 (C3H6)n由______种元素组成
(2)依据图1可知,熔喷布的质量与透气性的关系是___________
(3)熔喷布的细菌菌落总数需控制在______(CFU/g)以下。
(4)熔喷布的优点是_________
(5)下列说法中正确的是 ____
B 熔喷布内在质量需检测指标为:纵向断裂强力、横向断裂强力、静水压和透气性。
C 熔喷布中检出大肠菌群应在100(CFU/g)以下
D 熔喷布可用来制造医用防护服、手术衣、卫生巾等产品
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图为一些粒子的结构示意图和钠元素在元素周期表中的信息,请回答。

(1)A、B、C、D四种粒子中,属于阳离子的是__________(填字母,下同),这四种粒子中,属于相对稳定结构的是________________。
(2)F属于________元素(选填“金属”或“非金属”),其相对原子质量为___________。
(3)下列有关E和F的判断正确的是____________(填序号)。
①E可能是原子
②若E和F属于同种元素,则x=11
③若x=13,则E的粒子符号为A1
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】科学家成功合成新型催化剂,能将CO2高效转化为甲醇(CH3OH),该化学反应的微观过程如下图所示。下列说法正确的是
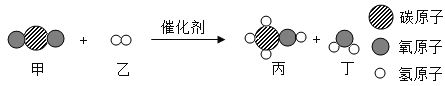
A.甲分子与丁分子的化学性质不同
B.甲醇分子中碳、氢原子个数比为1∶3
C.参加反应的甲、乙物质的质量比为22∶1
D.反应前后,原子的种类没有改变,个数改变
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】过氧化钙晶体(CaO2·nH2O)常温下为白色,能溶于酸,难溶于水、乙醇,是一种温和的氧化剂,常用于鱼类长途运输的增氧剂等。
l.过氧化钙晶体(CaO2·nH2O)的制备
实验室制备过氧化钙晶体反应方程式为CaCl2+H2O2+2NH3+nH2O=CaO2nH2O+2NH4Cl,实验装置如图。
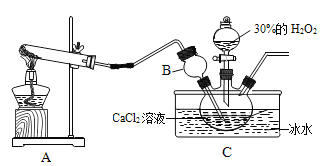
(1)装置A中生成的气体为______。
(2)装置B的作用是________。
(3)装置C采用冰水浴控制温度在0℃左右,可能的原因主要有:
①该反应是放热反应,温度低有利于提高CaO2nH2O产率;
②____。
(4)反应结束后,经过滤、洗涤、低温烘干可获得CaO2nH2O。检验晶体已洗涤干净的方法为______。
Ⅱ.过氧化钙晶体(CaO2nH2O)中n的测定
资料:CaO2nH2O加热至120℃完全失去结晶水,继续加热至350℃,剩余固体受热分解放出O2;
(5)某兴趣小组称取2.16g CaO2nH2O样品,用热分析仪对其进行热分解实验,测得剩余固体的质量随温度变化曲线如图所示

①CaO2nH2O中n的值为____。(写出计算过程)
②350℃发生反应的化学方程式为_________。
③若过氧化钙品体中混有杂质(杂质不参加反应),会导致测得的n的值___(填“偏大”“偏小”或“不变”)。
Ⅲ.过氧化钙晶体(CaO2nH2O)的性质研究
(6)该兴趣小组另称取少量CaO2nH2O样品于试管中,加入适量的稀盐酸使样品完全反应,然后加入足量的Na2CO3溶液,看到_____现象,说明CaO2nH2O与稀盐酸反应生成了CaCl2。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】硫酸是重要的化工原料。以火山喷发产生的硫磺(主要成分为S)作为原料生产硫酸的主要流程如下:
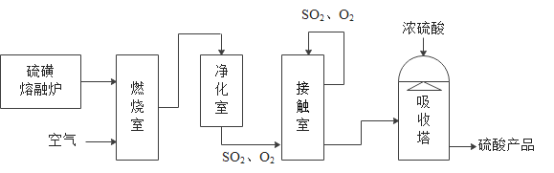
(1)接触室中,在催化加热条件下发生反应的化学方程式为_______________。
(2)上述流程中,涉及到的含硫物质有S、____________和 H2SO4。
(3)上述各物质中,硫元素呈现_______________种化合价。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据所学化学知识回答问题。
(1)在粗盐提纯的实验中其主要的操作步骤顺序是__(填数字序号)。
①过滤
②溶解
③蒸发
④计算产率
(2)在蒸发加热过程中,应用玻璃棒不断搅拌,防止因局部温度过高,造成___;当蒸发皿中出现_时,应停止加热。
(3)欲除去粗盐中可溶性杂质Na2SO4、MgCl2、 CaCl2 得到纯净的NaCl,所加试剂为稍过量的BaCl2溶液、稍过量的___ (填化学式) 溶液、稍过量的Na2CO3溶液和适量的稀盐酸。
(4)纯净的氯化钠是重要的化工产品,熔融态的氯化钠通电可生成金属钠和氯气,写出该反应的化学方程式__。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲、乙两种固体的溶解度曲线如图所示。
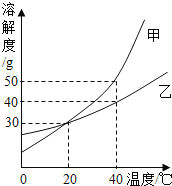
(1)小于20℃时,甲的溶解度______乙(填“>”、“=”或“<”);
(2)40℃时,若将55g甲(不含结晶水)放入100g水中充分溶解,得到______克溶液中甲的质量为______克;
(3)40℃时,将甲、乙两物质的饱和溶液各100g降温至20℃,析出晶体(均不含结晶水)的质量关系是:m(甲)______m(乙) (填“>”、“=”或“<”)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】燃烧是人类最早利用的化学反应之一,与我们的生活、社会的发展有着密切的联系。以下是关于燃烧的三个实验,请回答;
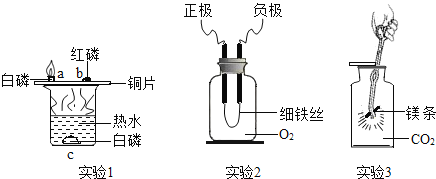
[实验1]a、b、c三处物质中能够燃烧的是______(填字母序号),其燃烧时伴随的现象是____。
[实验2]集气瓶中充满氧气,胶塞处装有一对石墨电极, 分别接到电源的正负两极,电极之间连有一段很细的铁丝。实验时,通入20V的直流电,能够看到铁丝剧烈燃烧。从燃烧的条件的角度分析产生以上现象的原因是________。
[实验3]将镁条在空气中点燃后再放入充满CO2的集气瓶中,发现镁条继续剧烈燃烧,发出白光,放热,产生一种白色固体和一种黑色固体。已知该反应为置换反应,则此白色固体和黑色固体分别是___。这个实验使你对燃烧条件产生的新认识是_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com