
 ĪŖĮĖ²ā¶Øij²»“æŠæ·Ūѳʷ֊ŠæµÄÖŹĮæ·ÖŹż£ØŌÓÖŹ²»ČÜÓŚĖ®£¬Ņ²²»ÓėĘäĖūĪļÖŹ·“Ó¦£©£¬Ä³»ÆѧŠ”×é½ųŠŠĮĖČēĻĀŹµŃ飬Ēė¼ĘĖć£ŗ
ĪŖĮĖ²ā¶Øij²»“æŠæ·Ūѳʷ֊ŠæµÄÖŹĮæ·ÖŹż£ØŌÓÖŹ²»ČÜÓŚĖ®£¬Ņ²²»ÓėĘäĖūĪļÖŹ·“Ó¦£©£¬Ä³»ÆѧŠ”×é½ųŠŠĮĖČēĻĀŹµŃ飬Ēė¼ĘĖć£ŗ·ÖĪö ŠæŗĶĻ”ĮņĖį·“Ӧɜ³ÉĮņĖįŠæŗĶĒāĘų£¬øł¾Ż·“Ó¦µÄ»Æѧ·½³ĢŹ½¼°ĘäĢį¹©µÄŠÅĻ¢æÉŅŌ½ųŠŠĻą¹Ų·½ĆęµÄ¼ĘĖćŗĶÅŠ¶Ļ£®
½ā“š ½ā£ŗ£Ø1£©Éś³ÉĒāĘųµÄÖŹĮæŹĒ£ŗ7g+100g-106.8g=0.2g£¬
¹ŹĢī£ŗ0.2£®
£Ø2£©Éčѳʷ֊ŠæµÄÖŹĮæĪŖx£¬
Zn+H2SO4ØTZnSO4+H2”ü£¬
65 2
x 0.2g
$\frac{65}{x}$=$\frac{2}{0.2g}$£¬
x=6.5g£¬
Ōѳʷ֊ŠæµÄ“æ¶ČĪŖ£ŗ$\frac{6.5g}{7g}$”Į100%=92.9%£¬
“š£ŗŌѳʷ֊ŠæµÄ“æ¶ČĪŖ92.9%£®
µćĘĄ ²īĮæ·ØŌŚ¼ĘĖćÖŠµÄÓ¦ÓĆŗܹć·ŗ£¬½ā“šµÄ¹Ų¼üŹĒŅŖ·ÖĪö³öĪļÖŹµÄÖŹĮæ²īÓėŅŖĒóµÄĪ“ÖŖŹżÖ®¼äµÄ¹ŲĻµ£¬ŌŁøł¾Ż¾ßĢåµÄŹż¾ŻĒó½ā£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ×ŌČ»½ēÖŠĖ®µÄĢģȻѻ·--Ė®·Ö×Ó²»¶ĻŌĖ¶Æ | |
| B£® | ĢģČ»Ęų¾Ń¹Ėõ“¢“ęŌŚøÖĘæÖŠ--Ń¹ĒæŌö“󣬷Ö×ÓÖ®¼äµÄ¼äøō±ä“ó | |
| C£® | µē½āĖ®Éś³ÉĒāĘųŗĶŃõĘų--ŌŚ»Æѧ·“Ó¦ÖŠ·Ö×Ó·¢Éśøıä | |
| D£® | ĶعżĘųĪ¶±ę±š¾Ę¾«ŗĶĖ®--·Ö×Ó²»¶ĻŌĖ¶Æ£¬²»Ķ¬·Ö×ӵĊŌÖŹ²»Ķ¬ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| Ń”Ļī | ĪļÖŹ£ØĄØŗÅÄŚĪŖŌÓÖŹ£© | ŹµŃé·½°ø |
| A | Ńõ»ÆĶ£ØľĢæ·Ū£© | ŌŚæÕĘųÖŠ³ä·Ö×ĘÉÕ |
| B | µŖĘų£ØŃõĘų£© | Ķعż×ĘČȵÄĶĶų |
| C | Ņų·Ū£ØŠæ·Ū£© | ¼ÓČė×ćĮæµÄĻ”ĮņĖį£¬¹żĀĖ”¢Ļ“µÓ”¢øÉŌļ |
| D | ĀČ»ÆÄĘČÜŅŗ£ØĀČ»ÆøĘ£© | ¼ÓČė×ćĮæµÄĢ¼Ėį¼ŲČÜŅŗ£¬¹żĀĖ |
| A£® | A | B£® | B | C£® | C | D£® | D |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 °“ÕÕČēĶ¼ĖłŹ¾½ųŠŠÖŠŗĶ·“Ó¦ŹµŃ飮
°“ÕÕČēĶ¼ĖłŹ¾½ųŠŠÖŠŗĶ·“Ó¦ŹµŃ飮²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
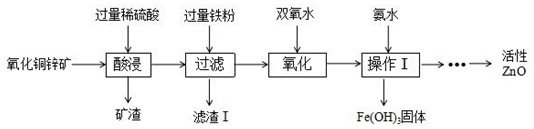
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 2Fe+3CuCl2=2FeCl2+3Cu | B£® | CuO+H2SO4=CuSO4+H3O | ||
| C£® | K2SO4+Ba£ØNO3£©2=BaSO4”ż+2KNO3 | D£® | Al£ØOH£©3+3HCl=AlCl3+3H2O |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¼ĘĖćĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® |  ĻØĆš¾Ę¾«µĘ | B£® | 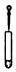 µĪ¼ÓŅŗĢå | C£® | 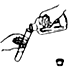 Ēćµ¹ŅŗĢå | D£® |  ³ĘĮæ¹ĢĢå |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
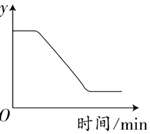 ŅŃÖŖ£ŗ2KClO3$\frac{\underline{MnO_2}}{”÷}$2KCl+3O2”ü£¬ČēĶ¼±ķŹ¾Ņ»¶ØÖŹĮæµÄKClO3 ŗĶMnO2¹ĢĢå»ģŗĻĪļŹÜČČ¹ż³ĢÖŠ£¬Ä³±äĮæyĖꏱ¼äµÄ±ä»ÆĒ÷ŹĘ£®×Ż×ų±ź±ķŹ¾µÄŹĒ£Ø””””£©
ŅŃÖŖ£ŗ2KClO3$\frac{\underline{MnO_2}}{”÷}$2KCl+3O2”ü£¬ČēĶ¼±ķŹ¾Ņ»¶ØÖŹĮæµÄKClO3 ŗĶMnO2¹ĢĢå»ģŗĻĪļŹÜČČ¹ż³ĢÖŠ£¬Ä³±äĮæyĖꏱ¼äµÄ±ä»ÆĒ÷ŹĘ£®×Ż×ų±ź±ķŹ¾µÄŹĒ£Ø””””£©| A£® | Éś³ÉO2µÄÖŹĮæ | B£® | ¹ĢĢåÖŠMnO2µÄÖŹĮæ | ||
| C£® | ¹ĢĢåÖŠŃõŌŖĖŲµÄÖŹĮæ | D£® | ¹ĢĢåÖŠ¼ŲŌŖĖŲµÄÖŹĮæ·ÖŹż |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com