
分析 硬水中含有较多的可溶性钙镁化合物,软水中不含或含有少量的可溶性钙镁化合物;根据净水的有关知识分析解答即可.
解答 解:(1)硬水软化就是减少水中的可溶性钙镁化合物,可溶性钙镁化合物受热易转化成不溶性钙镁化合物,故可以使用加热煮沸的方法降低水的硬度,故填:加热煮沸;
(2)小明同学用仪器测知该水质pH=5.9,pH值小于7,可知该水显酸性;
(3)A.水的污染会引起土壤污染,故A正确;
B.地球上淡水资源比较匮乏,故B错误;
C.明矾溶于水形成的胶体具有吸附性,能将水中不溶性固体杂质吸附在其表面形成大颗粒易于沉降,故C正确;
D.许多物质都能溶解在水中,水是一种很好的溶剂;故D正确;
故填:B.
(1)加热煮沸;(2)酸;(3)B.
点评 本题考查了净水的有关知识,水是人类宝贵的自然资源,我们要保护水,节约用水,完成此题,可以依据已有的知识进行.


 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案科目:初中化学 来源: 题型:解答题
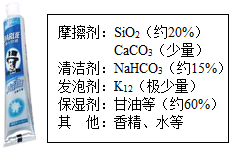 牙膏是生活必需品,某兴趣小组同学对某品牌市售牙膏展开如下探究,请回答问题.
牙膏是生活必需品,某兴趣小组同学对某品牌市售牙膏展开如下探究,请回答问题.| 实验编号 | 1 | 2 | 3 |
| 实验前/g | 2.00 | 2.00 | 2.00 |
| 实验后/g | 0.43 | 0.44 | 0.45 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 淀粉没有甜味,因此不属于糖类 | B. | 肥皂水可以区别硬水和软水 | ||
| C. | 生铁和钢都是铁的合金 | D. | 钢筋混凝土是复合材料 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| A. | 除去NaHCO3溶液中混有的Na2CO3,可以通入适量的二氧化碳 | |
| B. | 除去BaCl2溶液中的少量HCl,可以加入过量的BaCO3,然后过滤 | |
| C. | 某溶液中滴加稀盐酸,有气泡生成,将气体通入澄清石灰水变浑浊,该溶液中一定是碳酸根离子 | |
| D. | 在久置的某氢氧化钠溶液中滴加酚酞,溶液变红;再加入过量的氯化钡溶液,有白色沉淀生成,同时溶液变为无色.说明该氢氧化钠溶液已经部分变质 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 铜及其化合物一般都具有特征的颜色,例如Cu、Cu2O呈红色,CuO呈黑色,CuSO4•5H2O呈蓝色等.研究性学习小组甲为检测实验室用H2还原CuO所得红色固体中是否含有Cu2O进行了认真的探究.
铜及其化合物一般都具有特征的颜色,例如Cu、Cu2O呈红色,CuO呈黑色,CuSO4•5H2O呈蓝色等.研究性学习小组甲为检测实验室用H2还原CuO所得红色固体中是否含有Cu2O进行了认真的探究.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com