
小雨同学依据描述书写的化学符号:①3个锌原子;3ZN;②两个氢分子:2H2;③两个氢氧根离子:2OH-;④原子结构示意图 对应的粒子:Mg2+;⑤氯化亚铁的化学式:FeCl2;⑥-2价的氧元素:O2-。其中正确的有
对应的粒子:Mg2+;⑤氯化亚铁的化学式:FeCl2;⑥-2价的氧元素:O2-。其中正确的有
A. ②③⑤ B. ①⑤⑥ C. ②③④ D. ①③⑤
A 【解析】正确的有:②两个氢分子:2H2;③两个氢氧根离子:2OH-;⑤氯化亚铁的化学式:FeCl2;错误的有:①3个锌原子应为:3Zn;④原子结构示意图对应的粒子应为:Mg;⑥-2价的氧元素应为:。故选A。 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源:安徽省2018年中考化学 题型:单选题
为实现二氧化碳的绿色利用,科学家用固碳酶作催化剂设计了如下转化过程。下列有关说法正确的是
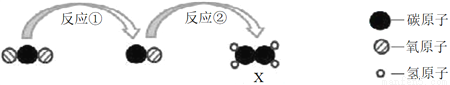
A. 反应①的化学方程式为CO2+C=CO B. 固碳酶在反应前后化学性质发生变化
C. X的化学式为CH2 D. 该过程实现了无机物向有机物的转化
D 【解析】A、该反应方程式缺少条件,故错误; B、固碳酶是催化剂,故反应前后的质量和化学性质不变,故错误; C、由图可知,X的化学式为C2H4,故错误; D、该过程实现了无机物向有机物的转化,正确。故选D。查看答案和解析>>
科目:初中化学 来源:重庆市2018年中考化学试卷(A卷) 题型:推断题
某工厂的废水中含有MgSO4和FeCl3,技术人员逐渐加入NaOH溶液调节废水的pH,先后分离出两种沉淀,并通过系列处理得到有价值的产品。操作流程如下图所示。

(1)固体A与某酸反应的化学方程式为____________。操作②时,当__________即可停止加热。
(2)固体B加热的产物是两种常见氧化物,则另一种氧化物的化学式为__________。
(3)溶液a除了可能含有NaOH外,还一定含有的溶质是_____________(填化学式)。
Mg(OH)2+H2SO4=MgSO4+2H2O 少量水(或析出大量晶体) H2O NaCl、Na2SO4 【解析】本题考查了酸、碱、盐的化学性质,混合物的分离等。根据物质的性质以及物质间的反应,结合化学方程式的书写的知识进行分析解答。 工业废水加入氢氧化钠溶液,会与硫酸镁反应生成氢氧化镁沉淀和硫酸钠,与氯化铁反应生成氢氧化铁沉淀和氯化钠,A中加入某酸后得到硫酸镁,则加入的酸是硫酸,固...查看答案和解析>>
科目:初中化学 来源:重庆市2018年中考化学试卷(A卷) 题型:单选题
安全事故无小事。下图是一种危险化学品警示标记,在运输时应张贴该标记的是

A. 食盐 B. 鞭炮 C. 烧碱 D. 酒精
C 【解析】A、食盐没有腐蚀性,在运输时不需张贴该标记,不符合题意;B、鞭炮在运输易发生爆炸,没有腐蚀性,在运输时不需张贴该标记,不符合题意;C、烧碱有腐蚀性,在运输时应张贴该标记,符合题意;D、酒精在运输易发生火灾,没有腐蚀性,在运输时不需张贴该标记,不符合题意。故选C。查看答案和解析>>
科目:初中化学 来源:湖北省黄冈市2018年中考化学试卷 题型:填空题
化学基础与常识
(1)下图金属应用的实例,主要利用金属的导热性的是_______(填序号);

A电缆 B.电热壶 C.金属丝 D.金属乐器
(2)向氢氧化钠溶液中滴加稀盐酸至恰好完全反应,反应前后溶液中存在的离子种类如图所示(其中“○”“ ”“●”“
”“●”“  ”表示不同离子)。则“○”与“
”表示不同离子)。则“○”与“ ”反应生成了_________(填物质名称)。
”反应生成了_________(填物质名称)。

(3)氢氟酸(HF)能刻画玻璃,其中有一个化学反应的化学方程式是: CaSiO3+6HF=X+SiF4↑+3H2O,则X的化学式为_______________
(4)氢能是一种极具发展潜力的清洁能。以太阳能为热源,热化学硫碘循环分解水是一种高效、无污染的制氢方法。其反应过程如图所示。

写出反应I中,发生反应的化学方程式:_____________________________。
B 水 CaF2 SO2+I2+2H2O=H2SO4+2HI 【解析】(1) A、电缆是利用金属的导电性,故错误;B、电热壶利用金属的导热性,故正确;C、金属丝利用金属的延展性,故错误;D、金属乐器利用金属具有金属光泽、硬度大,故错误;(2) 氢氧化钠与稀盐酸反应生成氯化钠和水,中和反应的实质是氢离子和氢氧根离子结合生成水分子;(3)在化学反应CaSiO3+6HF=X+SiF4↑+3H2O中...查看答案和解析>>
科目:初中化学 来源:广东省2018年中考化学试卷 题型:计算题
大型电动车使用的磷酸亚铁锂(LiFePO4)电池,具有“体积小、成本低、充电快、输出功率高、循环寿命长”等优点。回答问题:
(1)磷酸亚铁锂中非金属元素的原子个数比为_______。
(2)磷酸亚铁锂中锂、磷元素的质量比为_______。
(3)磷酸亚铁锂中铁元素的质量分数为________(精确到0.1%)。
P:O=1:4 7:31 35.4% 【解析】根据磷酸亚铁锂的化学式计算解答。(1)根据磷酸亚铁锂的化学式为LiFePO4,其中P、O属于非金属元素,故磷酸亚铁锂中非金属元素的原子个数比为P:O=1:4;(2)磷酸亚铁锂中锂、磷元素的质量比为7:31;(3)磷酸亚铁锂中铁元素的质量分数为×100%=35.4%。查看答案和解析>>
科目:初中化学 来源:广东省2018年中考化学试卷 题型:简答题
2017年冬天,某小伙子为了取暖在卫生间里贴满了“暖宝宝”(该产品的部分说明书为:“暖身更暖心,升温快。发热成分:高纯度铁粉、水、盐……;发热时间: 10小时;平均温度:52℃),他把门窗关闭以防暖气泄漏。几分钟后,他失去意识而倒地,幸而被门外的朋友及时救起。请回答:
(1)铁氧化发热,主要生成物的化学式为______;盐是催化剂,其质量和_____不变。
(2)该小伙子失去意识并不是温度过高和身体本身的原因,而是_____。
Fe2O3 化学性质 铁氧化消耗氧气,导致缺氧 【解析】(1)根据铁与氧气和水反应生成氧化铁解答;根据催化剂在化学反应中质量和化学性质都不变解答;(2)根据铁氧化发热需要消耗氧气解答。(1)铁与氧气和水反应生成氧化铁,化学式为Fe2O3;盐是催化剂,其质量和化学性质不变;(2)该小伙子失去意识并不是温度过高和身体本身的原因,而是铁氧化消耗氧气,导致缺氧。查看答案和解析>>
科目:初中化学 来源:湖南省衡阳市2018年中考化学试卷 题型:计算题
氯化钠是一种重要的化工原料。电解氯化钠溶液可制得氯气、氢氧化钠和氢气,反应的化学方程式为2NaCl+2H2O Cl2↑+H2↑+2NaOH。现取一定质量的氯化钠溶液进行电解,当氯化钠完全反应时,得到85.4g溶液,生成氢气的质量与时间的关系如图所示。请计算:
Cl2↑+H2↑+2NaOH。现取一定质量的氯化钠溶液进行电解,当氯化钠完全反应时,得到85.4g溶液,生成氢气的质量与时间的关系如图所示。请计算:

(1)氯化钠完全反应时生成氢气的质量是_________g。
(2)氯化钠完全反应时,生成氢氧化钠的质量是_________克?
(3)原氯化钠溶液中溶质的质量分数是_________?
0.4 16 23.4% 【解析】根据反应的化学方程式及其提供的数据计算解答。(1)由图可知:氯化钠完全反应时,生成氢气的质量是0.4g;(2)设生成氢氧化钠的质量是x,生成氯气的质量为y,氯化钠的质量为z。 2NaCl+2H2OCl2↑+H2↑+2NaOH 117 71 2 80 z y 0.4g x x=16g y=14.2g z=23.4g (...查看答案和解析>>
科目:初中化学 来源:云南省蒙自市业水平模拟考试(二)化学试卷 题型:填空题
(1)用化学用语填空。
① 氮元素 ___________。 ② 2个氦原子 __________。
③ 5个五氧化二磷分子__________。 ④ 氧化铝 __________。
⑤ 2个氢氧根离子 _________ 。
(2)说出NH3中 “3”的意义___________________________________。
N 2He 5P2O5 Al2O3 2OH - 每个氨分子中有3个氢原子(或一个氨气分子中有3个氢原子) 【解析】(1)①氮元素的元素符号为N;②原子的表示方法就是用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上相应的数字,所以2个氦原子,就可表示为 2He;③由分子的表示方法,正确书写物质的化学式,表示多个该分子,就在其化学式前加上相应的数字,则5个五氧化二磷分子可表示为:5...查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com