
科目:初中化学 来源: 题型:阅读理解
| ||
| ||
| ||
| 密度(ρ)/g?ml-1 | 1.00 | 1.02 | 1.04 | 1.06 | 1.08 | 1.10 | 1.12 | 1.14 | 1.16 | 1.185 |
| 溶质质量分数(w)/% | 0.4 | 4.4 | 8.5 | 12.5 | 16.5 | 20.4 | 24.2 | 28.2 | 32.2 | 37.2 |
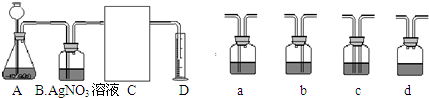
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源:2013-2014学年上海市嘉定区中考一模(即期末)化学试卷(解析版) 题型:探究题
在实验室配制100 g 10%的氯化铵溶液并探究酸碱性强弱与浓度及温度的关系。请回答有关问题:
(1)计算:需氯化铵的质量 g,水 mL;
(2)称量:用电子天平称取所需的氯化铵,用 (选填 “50mL”、 “100 mL”或“200mL”)的量筒量取所需水的体积;
(3)溶解:将上述称量好的氯化铵和水放到烧杯中,用玻璃棒搅拌,其作用是 。
(4)反思:若称取的氯化铵中含有水分或其它杂质,则所配制的氯化铵溶液的溶质质量分数会 。(选填“偏大”、“不变”或“偏小”)
(5)测溶液的酸碱性:用pH试纸测得氯化铵溶液的pH为5,则其为 性。为进一步探究其酸碱性的强弱与溶液的浓度、温度是否有关,采用以下四个步骤研究。请完成第二、第三步实验步骤。(不必写实验中涉及的仪器)
第一步:分别配制溶质质量分数为5%、10%、20%的氯化铵溶液;
第二步:在相同 下;分别测5%、10%、20%的氯化铵溶液的pH;
第三步: ;
第四步:根据测得数据,综合分析得出氯化铵溶液酸碱性的强弱与浓度、温度关系。
查看答案和解析>>
科目:初中化学 来源:云南 题型:单选题
| A.把NaOH固体直接放在天平托盘上称量 |
| B.将4gNaOH固体溶于196g水中 |
| C.用量筒量取200mL水溶解4gNaOH固体 |
| D.将配好的NaOH溶液放在烧杯中存放 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com