
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解

| 实验目的 | 实验操作 | 实验现象 |
| ①验证两种金属的活动性强弱 | (Ⅰ)取少量PdCl2溶液于小烧杯中,用镊子加入一小块金属锰. | 有黑色粉末生成,溶液由无色变为浅粉色(MnCl2). |
| (Ⅱ)取相同的稀硫酸于两个小烧杯中,分别放入两种金属. | 其中一支烧杯中有气体产生,溶液变为浅粉色,另一个烧杯中无明显现象. |
| 实验目的 | 实验操作 | 实验现象 |
| ② 探究钯在金属的活动性顺序的位置 探究钯在金属的活动性顺序的位置 |
(Ⅰ)取少量CuSO4溶液于一个小烧杯中,用镊子加入金属 钯 钯 ,一段时间后取出冲洗. |
无明显现象. |
| (Ⅱ)取少量AgNO3溶液于另一个小烧杯中,用镊子加入金属钯,一段时间后取出冲洗. | 无明显现象. | |
| (Ⅲ)取少量PdCl2溶液于第三个小烧杯中,加入老师提供的Pt丝. | 无明显现象. |
| 实验目的 | 实验操作 | 实验现象和结论 |
| 探究Mn和Zn的金属活动性强弱 |
查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解


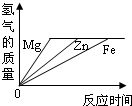
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com