
分析 (1)根据反应物、生成物的种类可以判断反应类型;
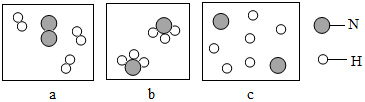
(2)反应过程中,氮气、氢气分解成氮原子、氢原子,氮原子和氢原子结合成氨分子;
(3)化学反应前后,元素种类不变,原子种类、总个数和质量都不变;
(4)如果氨气不慎泄露,防止引发危险,可关闭阀门,严禁明火并喷洒大量水雾,由此可知氨气可能具有的一条性质是易溶于水.
解答 解:(1)以上合成氨气的化学反应中,反应物是两种,生成物是一种,属于化合反应.
故填:化合.
(2)反应过程中,氮气、氢气分解成氮原子、氢原子,氮原子和氢原子结合成氨分子,则从反应开始到完成的排列顺序为a→c→b.
故填:a→c→b.
(3)由4NH3+3O2$\frac{\underline{\;点燃\;}}{\;}$2X+6H2O可知,反应前氮原子是4个,反应后应该是4个,包含在2X中,反应前后氢原子都是12个,氧原子都是6个,因此X是N2.
故填:N2.
(4)如果氨气不慎泄露,防止引发危险,可关闭阀门,严禁明火并喷洒大量水雾.由此可知氨气可能具有的一条性质是易溶于水.
故填:易溶于水.
点评 本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行分析、判断,从而得出正确的结论.


科目:初中化学 来源: 题型:选择题
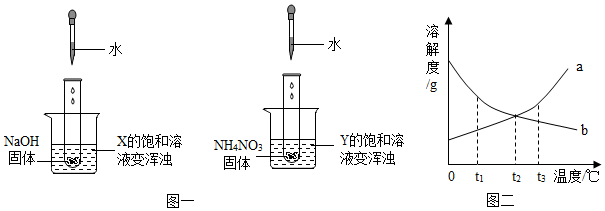
| A. | Y的溶解度曲线为b曲线 | |
| B. | 降温可使X的饱和溶液变浑浊 | |
| C. | X的饱和溶液从t2℃降温到t1℃,溶质的质量分数变大 | |
| D. | t3℃时,X、Y的饱和溶液质量相等,则溶剂质量X>Y |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A.物质组成 | B.物质构成 |
| 高锰酸钾、锰酸钾-组成元素相同 由一种元素组成的纯净物-单质 | 质子数-决定元素的种类 最外层电子数-决定元素的化学性质 |
| C.物质性质 | D.物质变化 |
| CO和CO2-都具有还原性 镁、铝、锌、铁-都能与稀盐酸反应 | 氢氧化钠去油污-化学变化 洗洁精去油污-物理变化 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
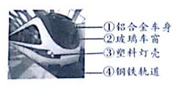 安徽合肥地铁1号线12月26日正式开通运营,这也标志着.合肥市民将迎来“地铁生活”,改变出现方式.如图是合肥地铁图:
安徽合肥地铁1号线12月26日正式开通运营,这也标志着.合肥市民将迎来“地铁生活”,改变出现方式.如图是合肥地铁图:查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com