
| A. | 铁和浓硫酸 | B. | 锌和稀硝酸 | C. | 铜和盐酸 | D. | 锌和稀硫酸 |
 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:选择题
| A. | 化合反应 | B. | 分解反应 | C. | 置换反应 | D. | 复分解反应 |
查看答案和解析>>
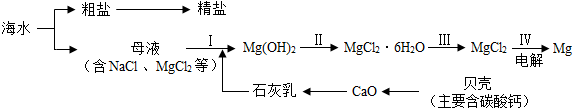
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 某化学兴趣小组的同学准备用氢气燃烧法测定空气中氧气的体积分数,设计的实验装置如图:
某化学兴趣小组的同学准备用氢气燃烧法测定空气中氧气的体积分数,设计的实验装置如图:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 琥珀酸亚铁由4个C原子、4H个原子、4个O原子、1个Fe原子构成 | |
| B. | 琥珀酸亚铁由4种元素组成 | |
| C. | 琥珀酸亚铁中C、O两种元素的质量比为1:1 | |
| D. | 琥珀酸亚铁的相对分子质量为172g |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验序号 | KClO3质量 | 其他物质质量 | 待测数据 |
| ① | 1.2g | / | |
| ② | 1.2g | CuO 0.5g | |
| ③ | 1.2g | MnO2 0.5g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com