
【题目】在利用红磷燃烧测定空气中氧气含量的实验中,用传感器记录集气瓶内氧气浓度随时间变化的情况,如图所示。

(进行实验)
活动1:证明红磷熄灭后,氧气还有剩余
实验装置 | 实验步骤 | 现象 | 结论 |
Ⅰ.用高能激光笔照射燃烧匙中足量的红磷 | 红磷燃烧,放出大量热,一段时间后熄灭,白磷始终不燃烧 | 红磷熄灭后,氧气还有剩余 | |
Ⅱ.冷却后,将装有白磷的燃烧匙提出水面,用高能激光笔照射 | 白磷 现象① |
(解释与结论)
(1)红磷燃烧的化学方程式为______________________。
(2)步骤Ⅰ中白磷始终不燃烧的原因是__________________。
(3)步骤Ⅱ中的现象①是_______________________。
(4)实验中气球的作用是_______________________。
活动2:探究影响剩余氧气浓度的因素
用如图装置进行实验,得到数据如表。
可燃物 | 白磷 | 红磷 | 木炭 |
着火点/℃ | 40 | 240 | 370 |
生成物状态 | 固态 | 固态 | 气态 |
剩余氧气浓度 | 3.1% | 7.0% | 14.0% |

(5)通过对比右表中红磷和白磷的相关数据,可以得出影响剩余氧气浓度的因素可能是________。
(6)结合以上探究及实验数据,在“测定空气中氧气含量”的实验中,通常使用红磷而不用木炭的原因可能有________。
【答案】4P+5O2![]() 2P2O5 未与氧气接触 燃烧 防止污染物进入空气,保护环境,还可以缓冲瓶内的压力 可燃物的着火点 木炭燃烧的生成物是气体,剩余氧气浓度较大
2P2O5 未与氧气接触 燃烧 防止污染物进入空气,保护环境,还可以缓冲瓶内的压力 可燃物的着火点 木炭燃烧的生成物是气体,剩余氧气浓度较大
【解析】
[解释与结论]
(1)红磷燃烧生成五氧化二磷,反应方程式为:4P+5O2![]() 2P2O5;
2P2O5;
(2)步骤Ⅰ中白磷始终不燃烧的原因是:未与氧气接触;
(3)步骤Ⅱ中的现象①是:白磷燃烧,因为白磷提出水面与氧气接触,温度达到白磷着火点,所以白磷燃烧。
(4)红磷燃烧生成的五氧化二磷会污染空气,气球的作用是:防止污染物进入空气,保护环境,还可以缓冲瓶内的压力;
(5)由图表数据可知,白磷和红磷比较,白磷着火点最低,瓶内剩余氧气最少,红磷着火点最高,瓶内剩余氧气最多,所以影响剩余氧气浓度的因素可能是可燃物的着火点;
(6)结合以上探究及实验数据,在“测定空气中氧气含量”的实验中,通常使用红磷而不用木炭的原因可能有:木炭燃烧生成物的气体,瓶中压强变化不大,无法测量消耗氧气的量,而且木炭燃烧完剩余氧气浓度大,测量结果不准确。


 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案科目:初中化学 来源: 题型:
【题目】向如图所示的容器中分层装填活性炭、小卵石、石英砂就制成了简易净水装置,有关说法正确的是( )
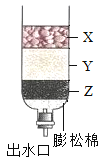
A.此装置能对水杀菌消毒B.此装置能降低水的硬度
C.X层装填石英砂D.Z层装填活性炭
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】兴趣小组欲探究Zn、Cu、Ag、R四种金属的活动性顺序(R为未知金属),进行了如下实验:
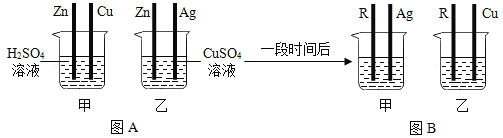
(1)如图A所示,将四根金属丝同时插入烧杯中,则甲中发生反应的化学方程式为 ,乙中的现象为 。
(2)一段时间后,将烧杯中四根金属丝依次替换为R、Ag、R、Cu,如图B所示,
① 若甲中出现气泡,乙中无明显现象,则烧杯乙中的物质是 ,可得出Zn、Cu、Ag、R的活动性顺序由强到弱为 ;
② 若甲中无明显现象,乙中R表面出现红色固体,则不能推出的结论是 。
a. R > Ag b. R > Cu c.R > Zn d.R < H
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学小组的同学们在探究“分子运动”时,设计了如下几组实验:
(实验装置)如图,实验1中的装置A取一个60 mL的试剂瓶,盖上一个单孔塞,单孔塞中插入一根带玻璃旋塞的导气管;装置B为一段医用输液管,内置一根浸泡过酚酞试剂并干燥的棉线。用橡胶管将A、B两装置链接。装置A 中加入约20 mL浓氨水,装置B的另一端连接导气管,导气管伸入小试管中。向小试管中加入一定量的蒸馏水。实验2、3、4的装置与实验1基本相同,只是根据实验需要变换了A、B装置和小试管的位置。
(实验步骤)①打开玻璃旋塞,观察现象。②将棉线润湿。
实验1 | 实验2 | 实验3 | 实验4 |
|
|
|
|
①干燥棉线没有明显变化。②湿润的棉线由a→b 逐渐匀速变红。 | 湿润的棉线由a→ b迅速变红,并且棉线变红的速率明显高于实验1 | 湿润的棉线由a→ b逐渐变红,并且棉线变红的速率明显低于实验1 装置。c→b 段棉线变红的速率比较缓慢,近b 端甚至不能变红。 | 湿润的棉线逐渐变红,并且a→b 段棉线变红的速率明显高于c→d 段棉线变红的速率 |
(1)以上实验得到的结论是:
①氨气不能使干燥的酚酞变色,氨气与水共同作用能够使酚酞试剂变红;
②_____;
③_____。
(2)若要应用实验1装置探究“温度对分子运动的影响”可以采取的操作是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】工业上常用“分离液态空气法”制氧气,此方法是以空气为原料,利用液氮与液氧沸点不同,将其分离。其微观示意图如下:
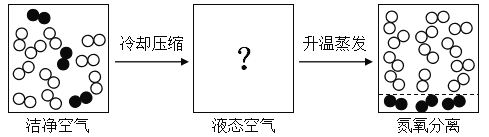
(1)“分离液态空气法”发生的是________(填“物理变化”或“化学变化”)。
(2)下列说法正确的是_______(填序号,下同)。
A洁净空气是纯净物 B此方法制氧气的原料来源广泛
C沸点属于物理性质 D利用此方法既可得到氧气又可得到氮气
(3)下列能表示液态空气微观示意图的是_____。
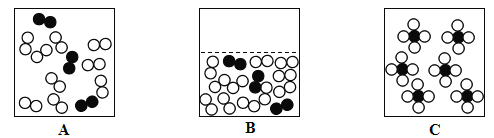
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】依据实验和溶解度曲线回答以下小题:
20℃时,向下列5只盛有100g水的烧杯中,分别加入不同质量的固体,充分溶解。
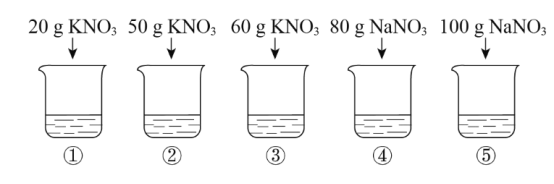
【1】上述溶液为饱和溶液的是
A.①②④B.①③⑤
C.②③⑤D.③④⑤
【2】④中溶液的质量为
A.80gB.100g
C.180gD.190g
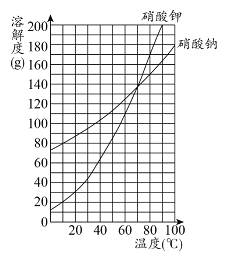
【3】下列温度中,KNO3比NaNO3溶解度大的是
A.30℃B.50℃
C.60℃D.90℃
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据下图所示的实验回答问题。
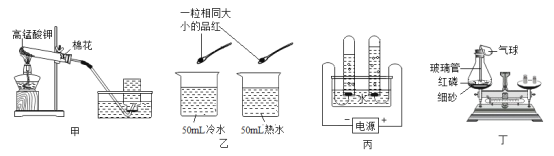
(1) 甲中棉花的作用是_____。
(2) 乙的目的是研究品红分子在水中的运动速率与_____的关系。
(3) 丙是电解水实验,反应的化学方程式为_____;与电源正极相连的试管中产生的气体是_____。
(4) 丁是验证质量守恒定律。其中红磷燃烧的化学方程式为_____;充分反应并冷却后,天平仍保持平衡,从微观的角度解释其原因:_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据如图所示的实验现象分析,下列说法错误的是
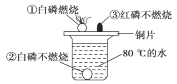
A. ①②对比说明物质燃烧需要与空气接触
B. ①中使温度达到白磷着火点是利用了铜的导热性
C. 烧杯中的热水只起提高温度的作用
D. ①③对比说明红磷着火点高于白磷
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】菱铁矿主要成分是碳酸亚铁(FeCO3),是一种分布广泛的矿物。某同学对碳酸亚铁和氧气充分反应后的固体成分进行了如下探究。
(查阅资料)① FeCO3在空气中加热生成铁的氧化物和二氧化碳。
②FeO是一种黑色粉末,在空气中加热,能迅速被氧化成四氧化三铁。Fe2O3能与盐酸反应生成氯化铁和水。Fe3O4能与盐酸反应生成氯化亚铁、氯化铁和水。
③酸性条件下,FeCl2能使高锰酸钾溶液褪色。向FeCl3溶液中滴加KSCN溶液,溶液变红色。
(猜想与假设)
猜想1:固体成分是Fe2O3 猜想2:固体成分是Fe3O4 猜想3:固体成分是FeO
(进行实验)
利用如图装置进行实验(加热和固定装置已略去,装置气密性良好)。
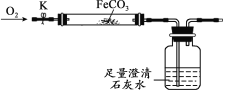
打开弹簧夹K,通入氧气,加热FeCO3。当瓶中产生的沉淀不再增加时,停止加热,继续通入氧气至玻璃管冷却。取玻璃管里的少量固体于试管中,滴加过量盐酸,微热,固体完全溶解。将所得溶液分成甲、乙两份进行实验。
实验编号 | 实验步骤 | 实验现象 |
a | 向甲溶液中滴加KSCN溶液 | 溶液变红色 |
b | 向乙溶液中滴加高锰酸钾溶液 | 高锰酸钾溶液的紫红色不消失 |
(解释与结论)
(1)在实验前就可以判断猜想________(填“1”“2”或“3”)不成立,因为___________。
(2)实验 b 的目的是_____________,由实验a、b的现象可知,猜想__________(填“1”“2”或“3”)成立,则FeCO3与氧气在加热时反应的化学方程式为________________。
(3)该同学反思后发现,不做实验a也能得出相同的结论,理由是___________________。
(拓展与应用)
(4)氧化铁是铁锈的主要成分,写出用盐酸除铁锈的化学方程式______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com