
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | |
| 溶解度/g | KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | 138 | 169 |
| NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | 37.8 | 38.4 | |
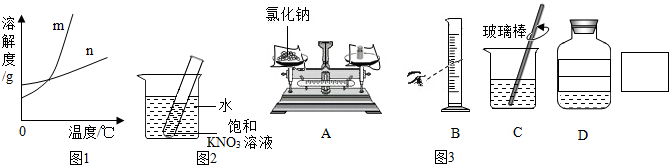
分析 根据溶液的配制的步骤、注意事项以及物质溶于水的能量变化、溶解度的知识进行分析解答即可.氯化钠的溶解度受温度影响变化不大;硝酸钾的溶解度随温度的升高而增大,故要析出硝酸钾的晶体需要降低温度;托盘天平在使用的时候,如果是已知称量物的质量,则需要先放好砝码和游码,且称量过程中不能再改变;仰视会导致量取的水多,从而所配溶液的溶质质量分数变小;在溶解过程中使用玻璃棒是为了加速溶解,据此解答.
解答 解:(1)根据表格提供的数据可以看出氯化钠的溶解度受温度影响变化不大,图1中能表示NaCl溶解度曲线的n,故填:n;
(2)20℃时,将盛有饱和KNO3溶液的小试管放入盛水的烧杯中,向水中加入某物质后,试管中有晶体析出,则会使温度降低,加入的物质可能是冰块和硝酸铵固体,故填:CD;
(3)①配制40g质量分数为5%的氯化钠溶液,溶质质量已知,则首先放好砝码和游码,故称量时A出现了右盘低的现象,接下来应该左盘中增加食盐,故填:D;
②量取水时,图B的方法是仰视读数,量取的水多,会使配制的溶液溶质质量分数偏小,故填:偏小;
③溶解中用玻璃棒搅拌的作用时加速溶解,若配制过程中,在已经有少量水的烧杯中加入氯化钠和水,则所得溶液中氯化钠的质量分数小于5%,故填:加速溶解;<.
④D中所贴标签应该注明溶液的名称和溶质质量分数,故填:氯化钠溶液,5%.
点评 本题考查的是溶解度以及溶液的配制的知识,完成此题,可以依据已有的知识进行.


科目:初中化学 来源: 题型:实验探究题
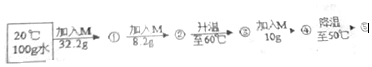
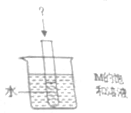 已知M物质和氯化钠的溶解度与温度的关系如表所示
已知M物质和氯化钠的溶解度与温度的关系如表所示| 温度/℃ | 20 | 30 | 40 | 50 | 60 | |
| 溶解度/g | 物质M | 32.2 | 37.4 | 40.4 | 50.4 | 55.2 |
| 氯化钠(NaCl) | 35.7 | 35.8 | 36 | 36.3 | 36.6 | |
查看答案和解析>>
科目:初中化学 来源: 题型:推断题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | O2和CO2分别通过灼热氧化铜 | B. | CO和CO2分别通入澄清石灰水 | ||
| C. | H2和CO2分别通入紫色石蕊试液 | D. | CO和O2分别通过灼热氧化铜 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com