
| 选项 | 实验目的 | 实验操作 |
| A | 除去CO2中少量的CO | 点燃 |
| B | 鉴别Cu和Fe3O4 | 观察颜色 |
| C | 鉴别H2O 和H2O2溶液 | 分别取少量液体于试管中,加入MnO2 |
| D | 除去CO中少量的CO2 | 通过足量的澄清石灰水 |
| A. | A | B. | B | C. | C | D. | D |
分析 A、依据少量的一氧化碳存在于二氧化碳中不易被点燃的原因进行分析;
B、根据铜是紫红色的,而四氧化三铁是黑色分析解答;
C、根据H2O2溶液和二氧化锰混合会放出氧气,而水和二氧化锰混合没有明显现象进行解答;
D、根据二氧化碳能够和氢氧化钙反应进行解答.
解答 解:A、不宜用点燃的方法除去CO2中的少量CO,是因为少量的一氧化碳在二氧化碳中可能不能燃烧,一般采用通过灼热的氧化铜来除去一氧化碳,故A错误.
B、铜是紫红色的,而四氧化三铁是黑色,所以可用观察颜色的方法鉴别Cu和Fe3O4,故B方法正确.
C、H2O2溶液和二氧化锰混合会放出氧气,而水和二氧化锰混合没有明显现象,故C方法正确;
D、二氧化碳能够和氢氧化钙反应,一氧化碳不能,因此可以通过足量的澄清石灰水除去CO中少量的CO2,故D方法正确.
故选:A.
点评 本题是一道鉴别及除杂题,解题的关键是利用鉴别与鉴定的基本原则,同时结合相关物质的性质对选项中的物质进行讨论即可.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 干冰升华时吸热,降低可燃物的着火点 | |
| B. | CO2不支持燃烧 | |
| C. | CO2覆在可燃物表面,隔绝空气 | |
| D. | 干冰升华后不污染档案资料 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
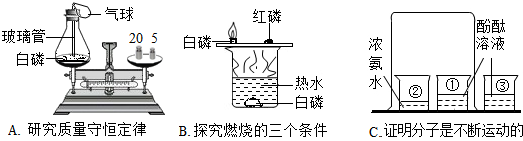
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 小明从超市购买了一些食品,发现生产厂家为了延长食品的保质期进行了不同的处理:
小明从超市购买了一些食品,发现生产厂家为了延长食品的保质期进行了不同的处理:查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
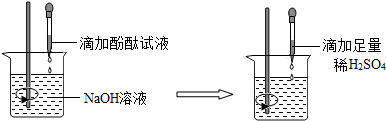
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com