
| A. | 木炭 | B. | 铁钉 | C. | 铁锈 | D. | 大理石 |
 教材全解字词句篇系列答案
教材全解字词句篇系列答案科目:初中化学 来源: 题型:选择题
 在探究我们吸入的空气和呼出气体有什么不同的活动中,用如图所示的方法收集一瓶呼出的气体,由此可以得出的结论是( )
在探究我们吸入的空气和呼出气体有什么不同的活动中,用如图所示的方法收集一瓶呼出的气体,由此可以得出的结论是( )| A. | 呼出的气体极易溶于水 | |
| B. | 呼出的气体易溶于水 | |
| C. | 呼出的气体不易溶于水 | |
| D. | 呼出的气体和吸入的空气成分是一样的 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 甲车间的污水中可能含有Ba2+和OH- | |
| B. | 乙车间的污水中可能含有Ag+和NO3- | |
| C. | 甲车间的污水中不可能含有Na+和Cl- | |
| D. | 乙车间的污水中不可能含有Fe3+和SO42- |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
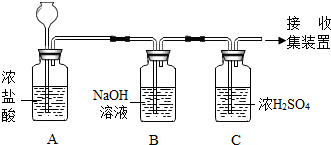 废物利用既可节约资源,又可以保护环境,如废旧干电池的金属中含有大量的锌,某课外兴趣小组设计了利用废旧干电池中的锌和浓盐酸以及下图所示的装置来制取干燥、纯净的氢气.试回答下列问题:
废物利用既可节约资源,又可以保护环境,如废旧干电池的金属中含有大量的锌,某课外兴趣小组设计了利用废旧干电池中的锌和浓盐酸以及下图所示的装置来制取干燥、纯净的氢气.试回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
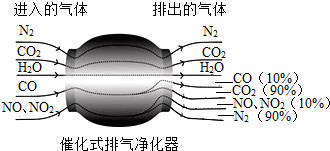
| A. | 在反应中CO作还原剂,氮氧化合物作氧化剂 | |
| B. | 在反应中N2、CO2、H2O起催化作用 | |
| C. | 净化器可有效降低温室效应 | |
| D. | 经净化器排出的气体对人类和环境不会造成危害 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 “化学反应条件的控制是实验的灵魂”.某校科学兴趣小组在老师指导下,进行了“探究影响金属活动性因素”的实验.请你帮助回答下列问题:
“化学反应条件的控制是实验的灵魂”.某校科学兴趣小组在老师指导下,进行了“探究影响金属活动性因素”的实验.请你帮助回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com