考点:金属的化学性质,二氧化碳的化学性质,碱的化学性质,酸碱溶液的稀释
专题:元素化合物知识型
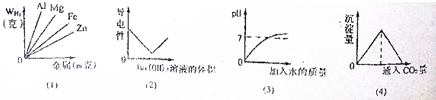
分析:A、在金属质量相同时,化合价也相同的条件下,相对分子质量越小的产生的氢气的质量越多,若化合价不同,则利用计算公式=
计算生成氢气的质量.
B、硫酸与氢氧化钡反应生成硫酸钡和水,随着氢氧化钡的加入,溶液中离子的浓度逐渐降低,导电性降低,当硫酸与氢氧化钡恰好反应时,溶液中的离子浓度几乎为零,导电性几乎为零,继续滴加氢氧化钡溶液,溶液导电性又增强.
C、硫酸显酸性,pH小于7,水的pH等于7,向一定量的H
2SO
4溶液中加水时,溶液的pH逐渐升高,但不会超过7.
D、澄清的石灰水中通入二氧化碳,先产生白色沉淀,后沉淀又消失.
解答:解:A、在金属质量相同时,化合价也相同的条件下,相对分子质量越小的产生的氢气的质量越多,若化合价不同,则利用计算公式=
计算生成氢气的质量,所以各种金属和酸反应产生氢气的质量是:镁
=0.083,铝
=0.11,铁
=0.036,锌
=0.03,所以产生氢气质量的由多到少的顺序是Al、Mg、Fe、Zn,故图象正确.
B、硫酸与氢氧化钡反应生成硫酸钡和水,随着氢氧化钡的加入,溶液中离子的浓度逐渐降低,导电性降低,当硫酸与氢氧化钡恰好反应时,溶液中的离子浓度几乎为零,导电性几乎为零,继续滴加氢氧化钡溶液,溶液导电性又增强,故图象正确;
C、硫酸显酸性,pH小于7,水的pH等于7,向一定量的H
2SO
4溶液中加水时,溶液的pH逐渐升高,但不会超过7,故图象错误;
D、石灰水中先通入二氧化碳,先发生Ca(OH)
2+CO
2═CaCO
3↓+H
2O,因此生成沉淀,后发生CaCO
3+CO
2+H
2O=Ca(HCO
3)
2,沉淀消失,且生成沉淀和溶解沉淀消耗的二氧化碳的质量比是1:1,故图象正确.
故选C.
点评:此题难度不大,明确发生的化学反应及反应与图象的对应关系是解题的关键.