
| 实验操作 | 实验现象 | 实验结论 |
将燃烧后的气体产物进行验证 | 甲中的白色固体变蓝 | 燃烧产物中有H2O |
| 乙装置质量增加 | 燃烧产物中有CO2 | |
| 丁中玻璃管内固体颜色变化是红色变成黑色、戊中澄清石灰水变浑浊 | 燃烧产物中有CO 写出丁中玻璃管内反应的化学方程式 Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2 |
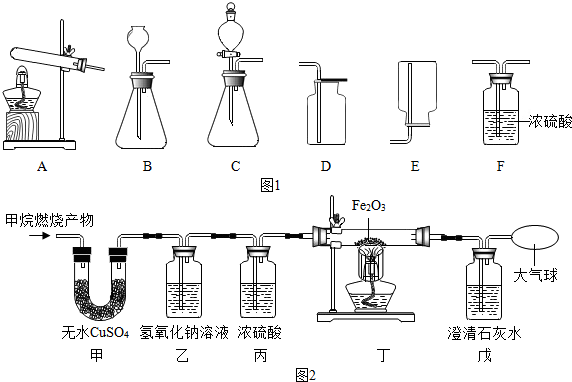
分析 制取装置包括加热和不需加热两种,如果用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集;氧气可以用浓硫酸干燥,收集干燥的氧气必须用向上排空气法收集,不能用排水法.用无水醋酸钠(化学式为CH3COONa)和碱石灰固体混合加热制取甲烷,因此需要加热;醋酸钠与氢氧化钠反应生成甲烷和碳酸钠.由题目的信息可知:无水硫酸铜吸水后变蓝,常用于吸收水和验证水的存在,因此甲装置是检验水的,乙装置质量增加说明有二氧化碳生成,如果将甲、乙装置顺序进行交换,则不能验证燃烧产物中有水生成,因为氢氧化钠溶液中有水;丁中玻璃管内固体颜色变化是红色变成黑色,戊中澄清石灰水变浑浊,说明生成了铁和二氧化碳,即一氧化碳和氧化铁在高温的条件下生成铁和二氧化碳,配平即可;根据甲装置增重求出氢元素的质量,求出甲烷的质量,再求出甲烷中的碳元素的质量,结合乙装置增重进而求出一氧化碳的质量,最后根据生成的二氧化碳和一氧化碳的个数比运用观察法进行配平;据此解答
解答 解:(1)用无水醋酸钠(化学式为CH3COONa)和碱石灰固体混合加热制取甲烷,因此需要加热;醋酸钠与氢氧化钠反应生成甲烷和碳酸钠;故答案为:A;CH3COONa+NaOH$\frac{\underline{\;\;△\;\;}}{\;}$CH4↑+Na2CO3;
(2)如果用双氧水和二氧化锰制氧气就不需要加热,氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集;氧气可以用浓硫酸干燥,收集干燥的氧气必须用向上排空气法收集;故答案为:CFD;
(3)由题目的信息可知:无水硫酸铜吸水后变蓝,常用于吸收水和验证水的存在,因此甲装置是检验水的,乙装置质量增加说明有二氧化碳生成,如果将甲、乙装置顺序进行交换,则不能验证燃烧产物中有水生成,因为氢氧化钠溶液中有水;丁中玻璃管内固体颜色变化是红色变成黑色,戊中澄清石灰水变浑浊,说明生成了铁和二氧化碳,即一氧化碳和氧化铁在高温的条件下生成铁和二氧化碳,配平即可;甲装置增重3.6g,即生成水3.6g,水中氢元素的质量=3.6g×2/18=0.4g,根据质量守恒定律,甲烷中的氢元素也是0.4g,因此甲烷的质量=0.4g÷4/16=1.6g,则甲烷中碳元素的质量=1.6g×12/16=1.2g,乙装置增重的2.2g是生成的CO2的质量,CO2的中碳元素的质量=2.2g×12/44=0.6g,因此一氧化碳中碳元素的质量=1.2g-0.6g=0.6g,则一氧化碳的质量=0.6÷12/28=1.4g,则生成的二氧化碳和一氧化碳的个数比1:1,根据此结果进行配平即可.
故答案为:①H2O;
②红色变成黑色;Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
③1.6;4CH4+7O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+2CO+8H2O
点评 本考点主要考查了气体的制取装置和收集装置的选择、气体的干燥,同时也考查了化学方程式的书写和有关的计算等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.


 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案科目:初中化学 来源: 题型:实验探究题
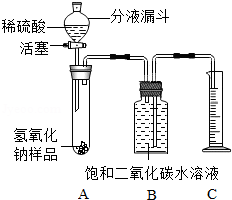 某化学课外小组的同学,为了测定实验室中一瓶因保存不善而部分变质的氢氧化钠中碳酸钠的质量分数,设计了如图所示的装置(图中铁架台已经略去),实验在27℃,101kPa下进行.
某化学课外小组的同学,为了测定实验室中一瓶因保存不善而部分变质的氢氧化钠中碳酸钠的质量分数,设计了如图所示的装置(图中铁架台已经略去),实验在27℃,101kPa下进行.| 实验步骤 | 实验现象 | 实验结论 |
| 1取样,溶于水,滴加过量的氯化钙溶液 | 产生白色沉淀 | 氢氧化钠部分变质 |
| 2静置,向上层清液中滴加酚酞溶液 | 变红色 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | 物质(括号内为杂质) | 试剂 | 操作方法 |
| A | FeSO4溶液(CuSO4) | 过量铁粉 | 过滤 |
| B | CO2气体(CO) | 足量氧化铁粉 | 高温加热 |
| C | CaO固体(CaCO3) | 足量的水 | 过滤 |
| D | NaCl固体(Na2CO3) | 足量稀盐酸 | 蒸发 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
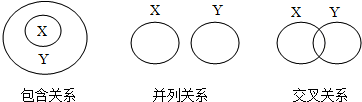
| A. | 纯净物与混合物属于包含关系 | |
| B. | 化合物与氧化物属于包含关系 | |
| C. | 单质与化合物属于交叉关系 | |
| D. | 金属元素和非金属元素属于并列关系 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 大量植树造林 | B. | 直接大量燃烧煤炭 | ||
| C. | 充分利用太阳能 | D. | 多骑自行车,少开汽车 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
 为探究铁锈蚀的影响因素,某兴趣小组做了如下实验.
为探究铁锈蚀的影响因素,某兴趣小组做了如下实验.查看答案和解析>>
科目:初中化学 来源: 题型:填空题
| 物质 | A | B | C | D |  |
| 分子示意图 |  |  |  |  |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com