
【题目】“砂锅鱼头”汤鲜汁浓,其烹饪方法为:将鱼头下油锅煎黄后,放入砂锅中加适量食盐、葱段、生姜、香菜、矿泉水等,在火上煨煮数小时即成。
(1)鱼头中的蛋白质进入人体后会逐步分解成被人体吸收的________。
(2)砂锅鱼头”中几乎不含有的营养素是________(填字序号)。
A 无机盐 B 油脂 C 糖类 D 水
(3)用洗洁精清洗油腻的砂锅是利用洗洁精的________作用。
(4)用液化气灶煨制砂锅鱼头时,砂锅外壁出现黑灰,此时可将灶具的进风口________(填“调大”或“调小”)。液化气的主要成分之一是丙烷(C3H8),丙烷完全燃烧的化学方程式为________3________8________2=________2________2________。
(5)使用液化气灶一定要注意安全,如果液化气一旦泄漏,遇到明火就可能发生爆炸。从微观角度解释发生爆炸的原因是________。
【答案】氨基酸 C 乳化 调大 C H +5O 3CO +4H O 液化气中的可燃性分子和氧气分子在点燃的条件下在有限的空间内剧烈燃烧生成水分子和二氧化碳分子并放出大量的热
【解析】
人体需要六类营养物质分别是糖类、脂肪、蛋白质、水、维生素、无机盐,丙烷在在氧气中燃烧生成二氧化碳和水,爆炸在极短时间内,释放出大量能量,产生高温,并放出大量气体,在周围介质中造成高压的化学反应或状态变化,同时破坏性极强。
(1) 氨基酸是蛋白质的基本组成单位,鱼头中的蛋白质进入人体后会逐步分解成被人体吸收的氨基酸。
(2) 人体需要六类营养物质分别是糖类、脂肪、蛋白质、水、维生素、无机盐,砂锅鱼头”中几乎不含有的营养素是糖类,故选C。
(3)用洗洁精清洗油腻的砂锅是利用洗洁精的乳化作用。
(4)用液化气灶煨制砂锅鱼头时,砂锅外壁出现黑灰,由于燃气燃烧不充分造成的,此时可将灶具的进风口调大,以利于燃气充分燃烧。液化气的主要成分之一是丙烷(C3H8),丙烷完全燃烧生成二氧化碳和水,化学方程式为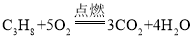 。
。
(5)使用液化气灶一定要注意安全,如果液化气一旦泄漏,遇到明火就可能发生爆炸。发生爆炸的原因是液化气中的可燃性分子和氧气分子在点燃的条件下在有限的空间内剧烈燃烧生成水分子和二氧化碳分子并放出大量的热。


科目:初中化学 来源: 题型:
【题目】欲用锌和稀硫酸反应制取氢气,然后利用氢气测定某CuO样品中含CuO的质量分数(假设杂质不挥发,也不发生反应),仪器的连接顺序为:B→A1→C→A2→A3。(已知:CuO+H2![]() Cu+H2O;其中 A1、A2、A3为3个浓硫酸洗气瓶)欲通过测量反应前后A2浓硫酸洗气瓶的质量变化来测算某CuO样品中含CuO的质量分数。
Cu+H2O;其中 A1、A2、A3为3个浓硫酸洗气瓶)欲通过测量反应前后A2浓硫酸洗气瓶的质量变化来测算某CuO样品中含CuO的质量分数。
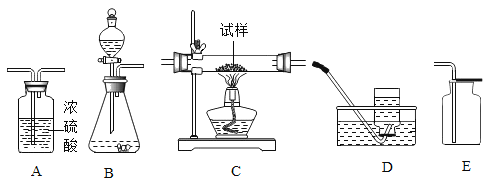
(1)C处大玻璃管内看到的主要实验现象是___________________。
(2)若测得洗气瓶A2的质量增加1.8g,则C处大玻璃管内的物质总质量应该减少____g。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室常用块状大理石和稀盐酸制取CO2气体。
(1)写出实验室制取CO2的化学方裎式:_______________。
(2)若用右图所示装置(固定装置省略)制CO:。连接好装置后, 需检查装置的气密性。具体操作方法是:先_______________(填字母,下同),后_______________若导管口有气泡,放手后导管内上升一段稳定的水柱,则气密性良好。
A.用手捂住试管 B.将导管一端浸入水中
(3)实验窒收集CO2可用的方法是_______(填字母)。
A.排水法 B.向下排空气法 C.向上排空气法
(4)实验室常用澄清石灰水检验CO2,写出反应的化学方程式:____________________。
(5)某些大理石中含少量硫化物,使制得的CO2中混有H2S气体。欲获取纯净、干燥的CO2,需对发生装置中产生的气体进行除杂,实验装置如下:
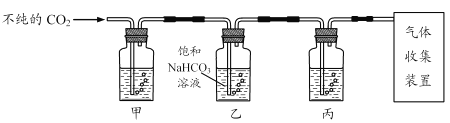
查阅资料:I.H2S能与NaOH等碱溶液、CuSO4溶液反应。
Ⅱ.CO2中混有的HC1气体可用饱和NaHCO3溶液吸收。
①装置甲中所盛试剂应选用_______(填字母)。
A.浓硫酸 B.NaOH溶液 C.澄清石灰水 D.CuSO4溶液
②装置丙的作用是____________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某校化学研究性学习小组探究气体制取的实验原理与方法.
(1)甲同学将课本的基础知识进行整理如图,请你帮助他完成相关内容.

制取气体 | 所需要品 | 装置连接顺序 | 反应的化学方程式 |
二氧化碳(干燥) | 大理石和稀盐酸 | ______________ | ______________________________ |
(2)乙同学设计的实验装置(如图),既可用于制取气体,又可用于验证物质性质.当打开K1、关闭K2时,利用I、Ⅱ装置可直接进行的实验是______________(填序号).

①大理石与稀盐酸反应制取二氧化碳
②锌与稀硫酸反应制取氢气
(3)丙同学认为在不改变I、Ⅱ、Ⅲ装置的仪器及
位置的前提下,该装置可用于过氧化钠(Na2O2)与水反应制取氧气,另一产物为氢氧化钠,则该反应的化学方程式为:______________________________;她的改进措施是_______________________________________________________.
(4)丁同学打开K2、关闭K1,利用I、Ⅲ装置来验证生成的二氧化碳中含有水蒸气,此时C中盛放的物质是_______________,可以观察到的现象是________________________________________.
(5)对用氯酸钾和二氧化锰的混合物制取O2后的固体残渣(假定已完全反应)作如下回收处理:
①通过以下四步实验操作回收二氧化锰.正确操作的先后顺序是____________(填写选项序号).
a.烘干b.溶解c.过滤d.洗涤
②用所得氯化钾晶体配制50g质量分数为5%的氯化钾溶液,需要氯化钾的质量为_______g.
③过滤、蒸发时都需用到的仪器是__________(填序号).
A.酒精灯B.烧杯C.玻璃棒D.漏斗E.量筒
(6)小明用6.5g可能含有铜、铝、铁、镁中的一种或几种金属杂质的锌粉,跟足量的稀盐酸完全反应时,生成0.2g氢气,则此锌粉中一定含有的金属杂质是________________.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某复合肥的部分说明书如图所示。请回答:

(1)从肥效的角度看,共有有效元素_____种。
(2)该复合肥的有效成分之一是硫酸铵[(NH4)2SO4],则硫酸铵中氮、氢、氧的原子个数比为__。
(3)一袋该化肥至少含N_______kg。
(4)从“注意事项”看,该复合肥料的物理性质是____,化学性质是_____(写一种)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】潜水器中可使用过氧化钠(Na2O2)固体做供氧剂,过氧化钠固体与二氧化碳反应原理是:2Na2O2+2CO2═2Na2CO3+O2,为验证该反应产物,某兴趣小组进行如下实验探究。
(查阅资料)过氧化钠与水反应生成氢氧化钠和氧气。
(设计实验)小组同学利用如图装置进行实(忽略稀盐酸的挥发)。
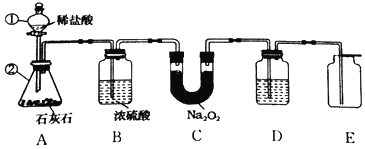
(1)装置A中标号仪器名称:①________,②________。
(2)装置A中反应的化学方程式为________。
(3)装置B的作用是________。
(4)为防止装置E收集的氧气中混有二氧化碳,装置D中盛放的试剂是________溶液。
(5)验证过氧化钠与二氧化碳反应产物
步骤 | 实验操作 | 实验现象 | 实验结论 |
① | 将带火星的木条伸入装置E中 | _____ | 产物中有氧气 |
② | 反应后取装置C中少量固体于试管中,加水完全溶解 | _____ | 固体中有未反应的过氧化钠 |
③ | 向步骤②反应后所得溶液中加入足量稀盐酸,有气体产生,将产生的气体通入足量澄清石灰水中 | _____ | 产物中有碳酸钠 |
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】从化学方程式![]() 中,可以获得的信息是( )
中,可以获得的信息是( )
A. MnO2遇到HCl就会反应
B. 生成的H2O和Cl2分子个数比为2:1
C. 生成物均为化合物
D. 反应前后锰元素的化合价不变
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】亚硝酸钠是实验室常用的试剂,实验室一般用亚硝酸钠溶液与氯化铵溶液反应来制取N2。N2的化学性质十分稳定,但在一定条件下能与H2部分化合生成NH3(转化率很低).下图为制取少量NH3的装置(制取H2的装置已略去):
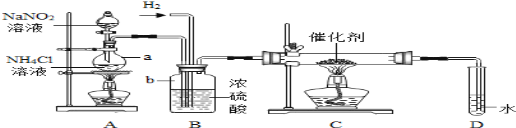
(1)指出标号仪器的名称a______,b______.
(2)A装置中除有N2生成外,还有水和氯化钠生成,写出反应的化学方程式__________.
(3)C装置的硬质试管中发生反应的化学方程式为_____________
(4)写出实验室制取H2的化学方程式___________,反应时N2和H2的最佳质量比是______,上述装置中是使产生平稳气流的方式是____________________
(5)B装置的作用是____________.(至少答两点)
(6)氨气极易溶解在水中,但是D装置却没有采用防倒吸装置,小丽认为装置没有错,理由是__________
(7)上述装置的缺陷是______________________
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】硝酸钾和氯化钠在不同温度下的溶解度如下表,请回答。
温度/℃ | 20 | 40 | 60 | 80 | 100 | |
溶解度/g | 硝酸钾 | 31.6 | 63.9 | 110 | 169 | 246 |
氯化钠 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 | |
(1)60℃时硝酸钾的溶解度是_____g。
(2)若硝酸钾中混有少量的氯化钠,提纯硝酸钾可以采取的方法是_____。
(3)20℃时,将硝酸钾和氯化钠两种固体各36g分别加入盛有100水的烧杯中,充分溶解后可观察到如图所示的现象。
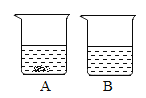
①烧杯A中溶解的物质是_____。
②若向烧杯A中加入一定量的水使剩余固体刚好全部溶解变为饱和溶液,则溶液中溶质的质量分数_____(填“变大”、“变小”或“不变”)。
③若将A、B烧杯中的物质同时升温至80℃,则A、B中溶质的质量_____(填“一定”或“不一定”)相等。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com