
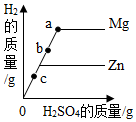
 两个烧杯中装有等质量的金属锌和镁,分别逐滴滴加同浓度的稀硫酸,产生氢气的质量与加入硫酸的质量关系如图所示.下列说法正确的是( )
两个烧杯中装有等质量的金属锌和镁,分别逐滴滴加同浓度的稀硫酸,产生氢气的质量与加入硫酸的质量关系如图所示.下列说法正确的是( )| A. | 该图说明镁比锌的金属活动性强 | |
| B. | a点时,两个烧杯中的酸都恰好完全反应 | |
| C. | b点时,两个烧杯中产生氢气的质量相同 | |
| D. | c点时,两个烧杯中都有金属剩余 |
分析 根据镁、锌金属活动性均比氢强,均能与稀硫酸反应,等质量的金属锌和镁,分别逐渐加入同浓度的稀硫酸,由生氢气的质量与加入硫酸的质量关系图,最终镁产生的氢气质量多,进行分析判断.
解答 解:A、由产生氢气的质量与加入硫酸的质量关系图,镁产生的氢气质量多,但无法得出镁与锌的金属活动性的关系,故选项说法错误.
B、a点时,镁与稀硫酸恰好完全反应,锌早已完全反应,故选项说法错误.
C、b点时,镁产生的氢气多,锌产生的氢气质量少,故选项说法错误.
D、c点时,锌与镁均还没有完全反应,两个烧杯中都有金属剩余,故选项说法正确.
故选:D.
点评 本题难度不大,理解产生氢气的质量与加入硫酸的质量关系图的含义,掌握金属的化学性质是正确解答本题的关键.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 含氧的化合物:氧化铜 氯酸钾 | B. | 单质:C60O3 | ||
| C. | 混合物:合金 金刚石 | D. | 化合物:甲烷 二氧化锰 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com