
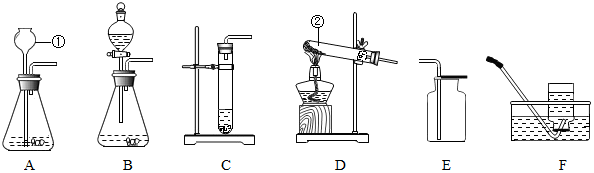
���� ��1������ʵ���ҳ������������ƺ�������ָ���������ý��з�����
��2�����ݹ��������ڶ������̵Ĵ������·ֽ�����ˮ����������Һ©�����Կ���Һ��ĵμ��ٶȣ�����ʵ�������濪���з�����
��3�����ݼ��Aװ�������Ե���ȷ�������з�����
��4���������������ڵ�ȼ�����������ɸ��µ��������������������ȵIJ���������з�����
��� �⣺��1��ͨ������������ָ���������ÿ�֪��������ƿ����������̨��
��2�����������ڶ������̵Ĵ������·ֽ�����ˮ����������ѧ����ʽΪ��2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2������Һ©�����Կ���Һ��ĵμ��ٶȣ�����ʵ�������濪�����Դӿ��Ʒ�Ӧ���ʺͽ�ԼҩƷ�ĽǶȿ��ǣ�����װ�����ѡ��B��
��3������װ��A��������ʱ���ӳ���©������ƿ�м�ˮ����û�¶˹ܿڣ���ֹˮ�м�ס��Ƥ�ܣ�������ˮ���γ�һ��ˮ������ˮ���߶ȱ��ֲ��䣬��װ��A�����������ã�
��4�����������ڵ�ȼ�����������ɸ��µ��������������������ȵIJ������壬�����ø�װ���ռ�����ʱӦע�⣺����ƿ��ҪԤ��һЩˮ��
�ʴ�Ϊ����1����ƿ������̨��
��2��2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2����B��
��3��ˮ���߶ȱ��ֲ��䣻
��4������ƿ��ҪԤ��һЩˮ��
���� ������Ҫ���鳣������ķ���װ�����ռ�װ�õ�̽��������װ�����ݷ�Ӧ���״̬�ͷ�Ӧ����ѡ���ռ�װ������������ܶȺ��ܽ���ѡ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ѡ�� | A | B | C | D |
| ʵ��Ŀ�� | ����ʳ��ˮ��ϡ���� | ������ë������ | ��������立�ĩ�������Ʒ�ĩ | �����Ȼ�狀�����[CO��NH2��2] |
| ʵ�鷽�� | �μ���ɫ��̪��Һ | ��������ζ | ��ˮ | ����ʯ����ĥ |
| A�� | A�� | B�� | B�� | C�� | C�� | D�� | D�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ��̽����

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ʵ������Ҫ�õ��IJ�����������ƽ���ձ�����Ͳ���������ͽ�ͷ�ιܵ� | |
| B�� | ���Ƹ�ϡ������Ҫ��ˮ800mL | |
| C�� | ����ϡ����ʱ�õ��������������������� | |
| D�� | ��ϡ�����У���Һ�������ܼ�����=5��4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ��̽����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ��̽����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ��̽����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
| Ũ���ᣨH2SO4�� 500���� | |
| Ũ�ȣ����������� | 98% |
| �ܶ� | 1.84��/���� |
| ��Է������� | 98 |
| ǿ��ʴ�ԣ����䣬�ܷ����� | |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com