
| 实验次数 | l | 2 | 3 | 4 |
| 取样品质量(g) | 50.0 | 50.0 | 50.0 | 50.0 |
| 取稀硫酸质量(g) | 40.0 | 80.0 | 120.0 | 160.0 |
| 产生气体质量(g) | 0.4 | 0.8 | 1.0 | 1.0 |
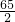 =
=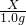 .
.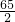 =
=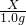 .
.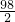 =
=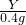 ,
,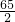 =
=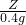 ,
, =
=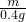 ,
,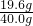 ×100%=49%;
×100%=49%;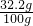 ×100%=32.2%.
×100%=32.2%. ×100%=70t,
×100%=70t, ×100%=35%,
×100%=35%,

科目:初中化学 来源: 题型:
| 实验次数 | l | 2 | 3 | 4 |
| 取样品质量(g) | 50.0 | 50.0 | 50.0 | 50.0 |
| 取稀硫酸质量(g) | 40.0 | 80.0 | 120.0 | 160.0 |
| 产生气体质量(g) | 0.4 | 0.8 | 1.0 | 1.0 |
| 65 |
| 2 |
| X |
| 1.0g |
| 65 |
| 2 |
| X |
| 1.0g |
查看答案和解析>>
科目:初中化学 来源:2012-2013学年黑龙江省哈尔滨市香坊区中考一模化学试卷(解析版) 题型:计算题
为测定黄铜(锌铜合金)样品的组成,某同学取四个样品分别加稀硫酸做了四次实验,其实验数据记录如下表..
|
实验次数 |
l |
2 |
3 |
4 |
|
取样品质量(g) |
50.0 |
50.0 |
50.0 |
50.0 |
|
取稀硫酸质量(g) |
40.0 |
80.0 |
120.0 |
160.0 |
|
产生气体质量(g) |
0.4 |
0.8 |
1.0 |
1.0 |
(1)反应的化学方程式
(2)列出计算黄铜中参加反应的金属质量(X)的比例式:
(3)参加反应的稀硫酸的溶质质量分数
(4)向第一次实验所得溶液中加入47.4g水,溶液中溶质的质量分数
(5)若工业上用125t含Cu2S 70%的辉铜矿炼制该黄铜,理论上能炼制出黄铜的质量为 。
查看答案和解析>>
科目:初中化学 来源:北京市期末题 题型:计算题

查看答案和解析>>
科目:初中化学 来源:2013年黑龙江省哈尔滨市香坊区中考化学一模试卷(解析版) 题型:解答题
| 实验次数 | l | 2 | 3 | 4 |
| 取样品质量(g) | 50.0 | 50.0 | 50.0 | 50.0 |
| 取稀硫酸质量(g) | 40.0 | 80.0 | 120.0 | 160.0 |
| 产生气体质量(g) | 0.4 | 0.8 | 1.0 | 1.0 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com