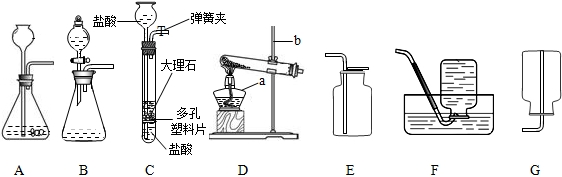
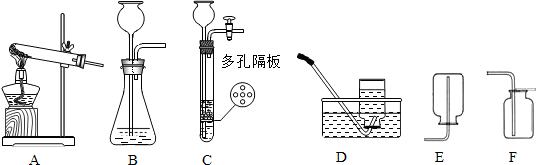
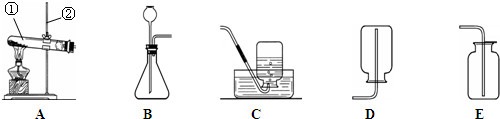
解:(1)由图示可知标号仪器a是酒精灯;
(2)由于粉末状的碳酸钙与盐酸的接触面积大,反应的速率快,难以控制.所以,在实验室里常用稀盐酸和块状大理石在装置A中反应制取二氧化碳,不用粉末状大理石,反应的方程式是:CaCO
3+2HCl═CaCl
2+H
2O+CO
2↑;
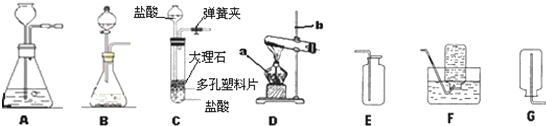
(3)由A、B、C三种装置的特点可知,C的优势是:能控制反应的发生和停止;
(4)实验室用加热无水乙酸钠固体和氢氧化钠固体制取甲烷,属于加热固体制取氧气,反应装置应选D;由于甲烷难溶于水,密度比空气小.收集装置可选用F或G;
(5)由于D装置属于加热固体制取取氧气,试管口没有加一团棉花,可用加热氯酸钾与二氧化们的混合物来制取氧气,反应的方程式是:2KClO
3 
2KCl+3O
2↑,由于氯酸钾反应放出氧气,混合物的质量减少,二氧化锰的分数增大.
故答为:(1)酒精灯;(2)粉末状石灰石和稀盐酸反应速率太快,难以控制,CaCO
3+2HCl═CaCl
2+H
2O+CO
2↑(3)能控制反应的发生和停止(4)D和F或G;(5)2KClO
3 
2KCl+3O
2↑,增大.
分析:(1)熟悉常见仪器的名称和用途;
(2)根据粉末状的碳酸钙与盐酸的接触面积大,反应的速率快分析,写出反应的方程式;
(3)对比A、B、C三种装置的特点,分析C装置的优点;
(4)根据实验室制取甲烷的反应物的状态和反应的条件确定发生装置,根据气体的收集方法确定收集装置;
(5)根据D装置的特点分析选择药品制取氧气,写出反应的方程式.根据氯酸钾反应放出氧气,混合物的质量减少分析二氧化锰的分数的变化.
点评:本题考查了常见仪器的名称、根据制取气体的装置选择制取的气体,只有熟练掌握实验室制取气体装置选择的依据才能解答好本题.

 2KCl+3O2↑,由于氯酸钾反应放出氧气,混合物的质量减少,二氧化锰的分数增大.
2KCl+3O2↑,由于氯酸钾反应放出氧气,混合物的质量减少,二氧化锰的分数增大. 2KCl+3O2↑,增大.
2KCl+3O2↑,增大.

 黎明文化寒假作业系列答案
黎明文化寒假作业系列答案