
 ij����ҩ���ı�ǩ��Ҫ������ͼ��ʾ��Ϊ�ⶨ�ø�Ƭ�����Ƿ���ϱ�ע��������ʵ�飺ȡ10Ƭ�ø�Ƭ���飬���˸���ྻ���ձ��У������ձ��м���50gϡ���ᣬǡ����ȫ��Ӧ����Ƭ�������ɷֲ�����ˮ��Ҳ����ϡ���ᷴӦ����Ӧ�в���������ȫ���ų�������Ӧ������ձ���ʣ�����ʵ�������Ϊ64.5g��
ij����ҩ���ı�ǩ��Ҫ������ͼ��ʾ��Ϊ�ⶨ�ø�Ƭ�����Ƿ���ϱ�ע��������ʵ�飺ȡ10Ƭ�ø�Ƭ���飬���˸���ྻ���ձ��У������ձ��м���50gϡ���ᣬǡ����ȫ��Ӧ����Ƭ�������ɷֲ�����ˮ��Ҳ����ϡ���ᷴӦ����Ӧ�в���������ȫ���ų�������Ӧ������ձ���ʣ�����ʵ�������Ϊ64.5g������ ��1�����������غ㶨�ɽ��з������ձ��е����ʼ��ٵ������������ɵĶ�����̼��������
��2�����ݶ�����̼�����������ݷ�Ӧ�ķ���ʽ�����̼��Ƶ��������������ÿƬ�иƵ������������жϸ�Ƭ�иƵĺ�����ע�Ƿ���ʵ��
��� �⣺��1����Ϊ̼��ƺ�ϡ���ᷴӦ�ų�������̼�����������غ㶨�ɿ�֪���ձ��е����ʼ��ٵ������������ɵĶ�����̼���������������ɶ�����̼������Ϊ��2g/Ƭ��10Ƭ+50g-64.5g=5.5g��
��2����10ƬƬ����̼��Ƶ�����Ϊx�����������е��Ȼ�������Ϊy��
CaCO3+2HCl�TCaCl2+H2O+CO2��
100 44
x 5.5g
$\frac{100}{x}$=$\frac{44}{5.5g}$
x=12.5g��
ÿƬ�иƺ�����12.5g��$\frac{40}{100}$��10Ƭ=0.5g��0.6g��ʵ�ʸƺ������ע�������
�ʴ�Ϊ����1��5.5g��
��2���������
���� ������Ҫ������������Ԫ�ص����á����������ļ��㣬���������غ㶨�������Ӧ�ų�������̼���������ǽ��к������Ļ��������ֳ�����֪ʶ���������������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
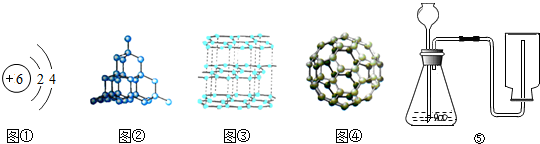
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ܽ��ܵ� | B�� | �������� | C�� | ����˫�� | D�� | ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ˮɹ�� | B�� | ��طŵ� | C�� | ��ѩ���� | D�� | �ɱ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
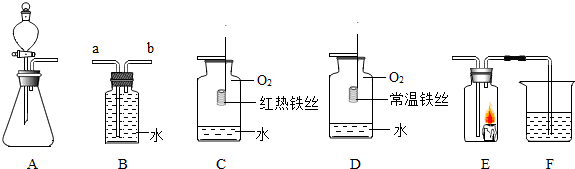
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �õ��ۡ����ǡ����㾫�Ȳ��ͳɡ����̷ۡ� | |
| B�� | �ù�ҵʯ�����������������ݡ� | |
| C�� | �����ȼ�պ������Ѭ����˿ | |
| D�� | �ý�ɫ��ˮ���εȶ��Ƴɡ��ٽ��͡� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ����ʾ�������ʿ��Է�����Ӧ���á�
����ʾ�������ʿ��Է�����Ӧ���á� ����ʾһ�����ʷ�Ӧ������һ�����ʣ���ͼ��ʾ����֪��A��E�ܷ����û���Ӧ��B��A��C��Ӧ�����������ɣ�
����ʾһ�����ʷ�Ӧ������һ�����ʣ���ͼ��ʾ����֪��A��E�ܷ����û���Ӧ��B��A��C��Ӧ�����������ɣ�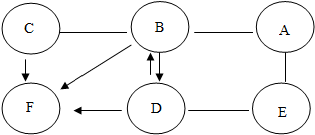
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com