
| A、洗涤剂可乳化餐具上的油污 |
| B、用灼烧法鉴别棉纤维和羊毛纤维 |
| C、氢氧化钠溶液可直接用作厨房清洁剂 |
| D、长期用硬水洗涤的衣物会变硬 |


科目:初中化学 来源: 题型:
| ||
| △ |
| A、一氧化氮(NO)的化学性质稳定 |
| B、上述含氮物质中氮元素的化合价有3种 |
| C、制取硝酸过程中产生的NO可循环使用 |
| D、①为置换反应;②为化合反应;③为复分解反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| A、硫粉在空气中燃烧时,发出蓝紫色火焰,生成具有刺激性气味的气体 |
| B、浓硫酸的试剂瓶口能看到大量的白雾 |
| C、木炭在氧气中燃烧,生成黑色固体 |
| D、将CO2通入紫色石蕊溶液中,溶液变为红色 |
查看答案和解析>>
科目:初中化学 来源: 题型:

| A、x、y、z、w均为化合物 |
| B、该反应属于置换反应 |
| C、该反应中y与w的质量比为1:2 |
| D、该反应的化学方程式是2NaClO2+Cl2=2NaCl+2ClO2 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| A、金刚石、石墨和C60都是由碳原子构成的单质 |
| B、铁锈覆盖在铁的表面,保护里层的铁不再与氧气反应 |
| C、生铁的含碳量比钢高 |
| D、pH为6的雨水属于酸雨 |
查看答案和解析>>
科目:初中化学 来源: 题型:
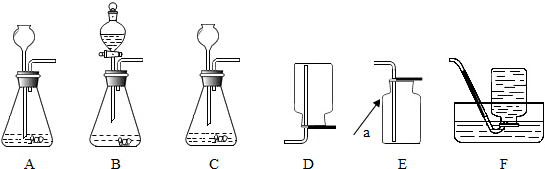
查看答案和解析>>
科目:初中化学 来源: 题型:
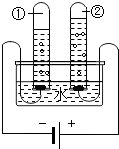 化学研究物质的组成、结构、性质、变化之间的关系.
化学研究物质的组成、结构、性质、变化之间的关系.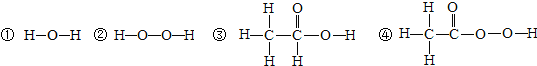
查看答案和解析>>
科目:初中化学 来源: 题型:
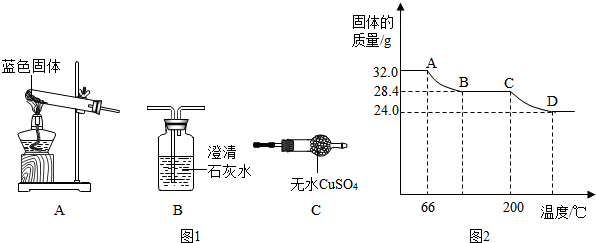
查看答案和解析>>
科目:初中化学 来源: 题型:
| A、①为置换反应 |
| B、钴的金属活动性比铜强 |
| C、②为复分解反应 |
| D、Co(OH)2可以干燥氯化氢气体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com