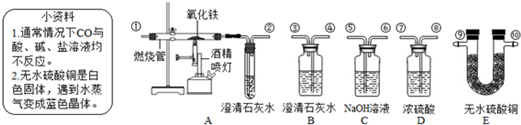
ÒŃÖȘČĘËᣚH
2C
2O
4Ł©ÔÚŒÓÈÈÌőŒțÏ»᷹Éú·Öœâ·ŽÓŠŁŹÍŹŃ§ĂǶÔÉúłÉÎïČúÉúÁËĆšșń”ÄĐËÈ€ŁŹÓÚÊÇÓĂÊ”Ńé”Ä·œ·š¶ÔÉúłÉ”ÄÎïÖÊœűĐĐÌœŸżŁź
[ÌáłöČÂÏë]ČúÉú”ÄÆűÌćÊÇÒ»Ńő»ŻÌŒĄą¶țŃő»ŻÌŒșÍËźŐôÆű”Ä»ìșÏÎïŁź
[ČéÔÄŚÊÁÏ]ŒîÊŻ»ÒÊÇčÌÌćÇâŃő»ŻÄÆșÍŃő»ŻžÆ”Ä»ìșÏÎïŁź
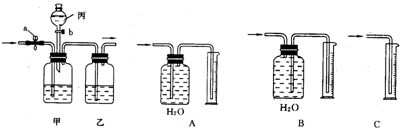
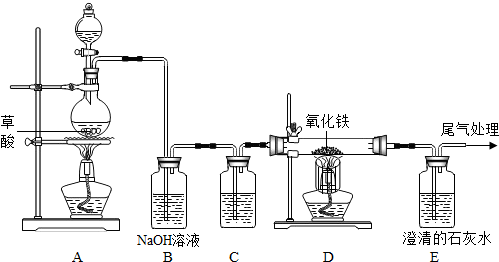
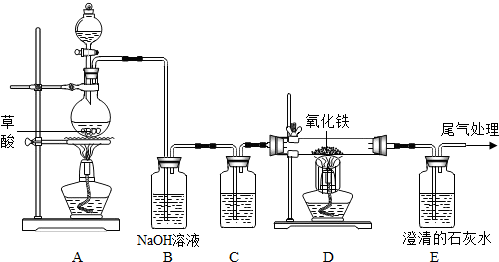
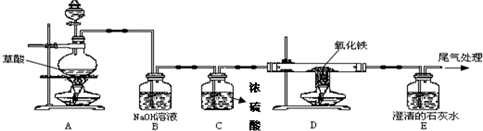
[Ê”ŃéčęłÌ]͏ѧĂÇŸčęÌÖÂÛÉèŒÆÁËÈçÏÂÍŒËùÊŸŚ°ÖĂŁŹČąœűĐĐÁËÊ”Ń飚ȿ·ÖŒĐłÖÒÇÆśÒŃÂÔÈ„Ł©Łź
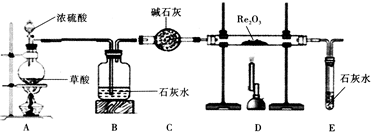
Łš1Ł©čÛČ씜Ś°ÖĂDÖĐČúÉú”ÄÏÖÏóÎȘ
șìÉ«”Ä·ÛÄ©Öđœ„±äłÉșÚÉ«
șìÉ«”Ä·ÛÄ©Öđœ„±äłÉșÚÉ«
ŁŹĐŽłöŽË·ŽÓŠ”Ä»ŻŃ§·œłÌÊœ
Łź
Łš2Ł©Ś°ÖĂC”ÄŚśÓĂÎȘÎüÊŐ»ìșÏÆűÌćÖĐ”ÄËźșͶțŃő»ŻÌŒŁŹÆäÖĐŃő»ŻžÆÓëËź·ŽÓŠ”Ä»ŻŃ§·œłÌÊœÎȘ
CaO+H2O=CaŁšOHŁ©2
CaO+H2O=CaŁšOHŁ©2
Łź
Łš3Ł©čÛČ씜Ś°ÖĂBÖĐłÎÇćÊŻ»ÒËź±ä»ëŚÇŁŹĐŽłöŽË·ŽÓŠ”Ä»ŻŃ§·œłÌÊœ
CO2+CaŁšOHŁ©2=CaCO3Ąę+H2O
CO2+CaŁšOHŁ©2=CaCO3Ąę+H2O
ŁŹÓɎ˔óö”ÄœáÂÛÎȘ
ČĘËá·ÖœâČúÉú”ÄÆűÌćÖĐșŹÓĐCO2
ČĘËá·ÖœâČúÉú”ÄÆűÌćÖĐșŹÓĐCO2
ŁźÓÖÖȘŚ°ÖĂC”ÄÖÊÁżÔöŒÓÁËŁŹEÖĐÊŻ»ÒËź±ä»ëŚÇÁËŁŹČąœáșÏÉÏÊöÊ”ŃéÏÖÏóŁŹÄłÍŹŃ§”ĂłöÁËœáÂÛŁź
[”ĂłöœáÂÛ]͏ѧÈÏÎȘČÂÏëŐęÈ·ŁŹÇëĐŽłöČĘËá·Öœâ”Ä·œłÌÊœ
Łź
[·ŽËŒÓëÆÀŒÛ]Łš1Ł©ÓĐ͏ѧÈÏÎȘÉÏÊöÊ”ŃéÓĐČ»ŚăÖźŽŠŁŹÄăÈÏÎȘÏÂÁĐœšÒéŐęÈ·”ÄÊÇ
ąÙąÚąÜ
ąÙąÚąÜ
ŁšÌîÊęŚÖĐòșĆŁ©ŁźąÙÓŠÔÚŚ°ÖĂAĄąBÖźŒäÔöŒÓŒìŃéËźŐôÆű”ÄŚ°ÖĂŁ»ąÚÓŠÔÚŚ°ÖĂEșóÔöŒÓÎČÆűŽŠÀ팰ÖĂŁ»ąÛżÉœ«Ś°ÖĂC»»łÉŚ°ÓĐĆšÁòËá”ÄÏŽÆűÆżŁ»ąÜŚ°ÖĂCĄąDÖźŒäÔöŒÓÊąÓĐłÎÇćÊŻ»ÒËź”ÄÏŽÆűÆżn
Łš2Ł©ÄłÁ¶Ìúł§ĂżÌìÏûșÄ5000tșŹŃő»ŻÌú76%”ÄłàÌúżóÊŻŁŹžĂł§ÀíÂÛÉÏżÉÈŐČúŽżÌú”ÄÖÊÁżÊǶàÉÙŁż




 ÓĆÖÊżÎÌĂżìÀֳɳ€Ï”ÁĐŽđ°ž
ÓĆÖÊżÎÌĂżìÀֳɳ€Ï”ÁĐŽđ°ž