
分析 (1)根据化合物中各元素质量比=各元素的相对原子质量×原子个数之比进行解答;
(2)据反应前后原子的种类和数目不变求物质的化学式,然后根据化学式进行计算.
解答 解:(1)氨气(NH3)中氮元素与氢元素的质量比为14:(1×3)=14:3,故填:14:3;
(2)化学反应前后原子的种类和数目不变,NH3+CO2+H2O+NaCl=NaHCO3+A,反应物中有氮原子1个,氢原子5个,氧原子3个,碳原子1个,钠原子1个,氯原子1个,而生成物中有钠原子1个,氢原子1个,碳原子1个,氧原子3个,所以还需氢原子4个,氮原子1个,氯原子1个,而A是一种氮肥,所以其化学式为NH4Cl;50kgNH4Cl中含氮元素的质量为:50kg×$\frac{14}{14+1×4+35.5}×100%$=13.1kg;故填:13.1.
点评 本题难度不大,考查同学们灵活运用化学式的有关计算进行分析问题、解决问题的能力.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 空气是由氧气、氮气、二氧化碳这三种气体构成的 | |
| B. | 空气中的二氧化碳可以用作灭火剂 | |
| C. | 焊接金属时常用作保护气的氮气不可以用分离液态空气的方法分离出来 | |
| D. | 空气中的氧气为白色气体 |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
 某化学兴趣小组的同学取来50g某建筑废料于烧杯中,然后向烧杯中加入足量的8%稀盐酸进行反应,烧杯中剩余固体的质量与加入盐酸质量的关系如图所示.求:(假设该建筑废料中只有CaCO3与酸反应)
某化学兴趣小组的同学取来50g某建筑废料于烧杯中,然后向烧杯中加入足量的8%稀盐酸进行反应,烧杯中剩余固体的质量与加入盐酸质量的关系如图所示.求:(假设该建筑废料中只有CaCO3与酸反应)查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | K+、SO42-、OH- | B. | Cl-、K+、CO32- | C. | K+、Cu2+、NO3- | D. | Ba2+、SO42-、K+ |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验步骤 | 实验现象 | 实验结论 |
| ①取少量该混合液于试管中 加入氢氧化钠溶液,振荡,过滤, 用蒸馏水洗涤滤渣; ②取洗涤后的滤渣加入稀硝酸. | 有白色沉淀生成,加入硝酸后,沉淀溶解 | 得到硝酸镁溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
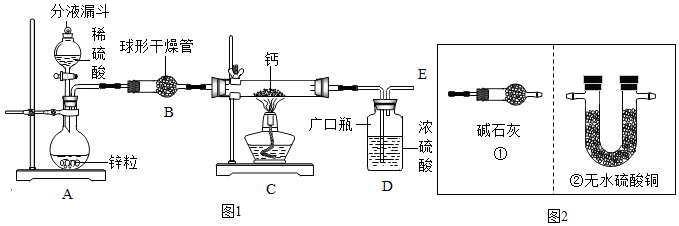
| 实验步骤 | 预期现象和结论 |
| 取少量固体样品,在干燥条件下与氧气反应,将 其产物通入装有无水硫酸铜的干燥管; | 若观察到无水硫酸铜变蓝色,证明是氢化钙,反之是钙 |

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com