
| A. | 硬水洗涤衣物适宜使用肥皂 | |
| B. | 二氧化锰可作所有反应的催化剂 | |
| C. | 吸入甲醛或一氧化碳会危害人体健康 | |
| D. | 铝合金与钢铁相比具有密度大、易腐蚀的特点 |
 小学教材全测系列答案
小学教材全测系列答案科目:初中化学 来源: 题型:选择题
| 序号 | 物质 | 所含杂质 | 除杂试剂 |
| A | HCl | CO2 | 适量NaOH溶液 |
| B | CaCO3 | CaCl2 | 适量稀盐酸 |
| C | 盐酸 | 稀硫酸 | 适量AgNO3溶液 |
| D | ZnSO4溶液 | CuSO4溶液 | 适量锌粉 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 物 质 | 所含杂质 | 除去杂质的试剂或方法 | |
| A | NaCl溶液 | Na2CO3 | 过量盐酸,加热 |
| B | CuO | Cu | 灼烧 |
| C | KCl | KClO3 | MnO2,加热 |
| D | O2 | H2O | 浓硫酸,干燥 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 步骤 | 现象 | 结论 |
| 取少量溶液a,滴加氯化铜溶液 | 溶液中无蓝色絮状沉淀 | 不含氢氧化钠 |
| 方案 | 步骤 | 现象 |
| 一 | 取少量溶液a,滴加硝酸银溶液 | 产生白色沉淀 |
| 二 | 取少量溶液a,加入镁粉 | 产生气泡 |
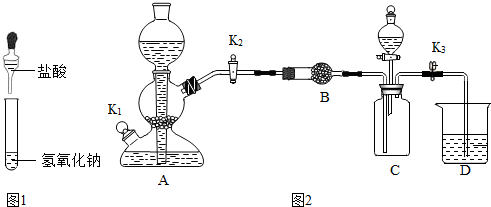
| 液体 | 步骤 | 现象 |
| 水 | 打开分液漏斗活塞,加入液体后关闭活塞 | D中导管先有气泡冒出,后D中石蕊试液倒流较少或D中导管倒吸一段水柱 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com