


 一课一练课时达标系列答案
一课一练课时达标系列答案科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源:2010届北京市大兴区中考二模化学试卷(解析版) 题型:信息分析题
(7分) 利用金属及金属活动性顺序的有关知识解决下列问题。
(1)某兴趣小组的同学学习了金属的性质后,在实验室找到的一种银白色金属R做如下探究:
①将金属R投入稀盐酸中,金属表面有气泡冒出。则该金属R在金属活动性顺序表中排在氢的 (选填“前面”或“后面”)。
②将金属R投入到FeSO4溶液中,金属R表面有黑色物质析出。根据上述信息,判断金属Fe、R、Cu活动性由强到弱的顺序是 。
(2)工业生产中常用10%的稀盐酸来除铁制品表面的铁锈,写出盐酸除铁锈反应的化学方程式 ;若要配制该盐酸600g,则需要溶质质量分数为40%的浓盐酸(密度为1.2g/mL) mL。
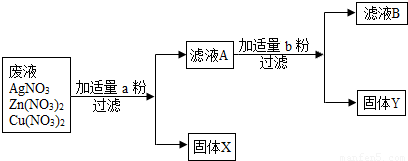
(3)某校实验室废水中含有Zn(NO3) 2、AgNO3、Cu(NO3) 2三种物质。该校化学兴趣小组的同学为了从中分离、回收金属Ag和Cu,设计了如下实验方案(实验中未引进其它金属离子):
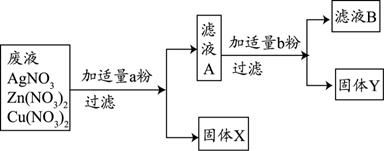
回答问题:
①固体X是 。
②写出实验过程中所发生反应的化学方程式 。
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:
利用金属及金属活动性顺序的有关知识解决下列问题。
(1)某兴趣小组的同学学习了金属的性质后,在实验室找到的一种银白色金属R做如下探究:
①将金属R投入稀盐酸中,金属表面有气泡冒出。则该金属R在金属活动性顺序表中排在氢的 (选填“前面”或“后面”)。
②将金属R投入到FeSO4溶液中,金属R表面有黑色物质析出。根据上述信息,判断金属Fe、R、Cu活动性由强到弱的顺序是 。
(2)工业生产中常用10%的稀盐酸来除铁制品表面的铁锈,写出盐酸除铁锈反应的化学方程式 ;若要配制该盐酸600g,则需要溶质质量分数为40%的浓盐酸(密度为1.2g/mL) mL。
(3)某校实验室废水中含有Zn(NO3) 2、AgNO3、Cu(NO3) 2三种物质。该校化学兴趣小组的同学为了从中分离、回收金属Ag和Cu,设计了如下实验方案(实验中未引进其它金属离子):
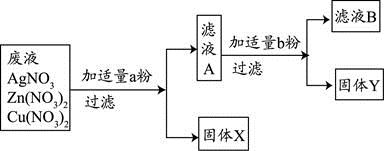
回答问题:
①固体X是 。
②写出实验过程中所发生反应的化学方程式 。
查看答案和解析>>
科目:初中化学 来源:2010年北京市大兴区中考化学二模试卷(解析版) 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com