

 应用题作业本系列答案
应用题作业本系列答案科目:初中化学 来源:不详 题型:实验题

查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题
| 实验操作 | 实验现象 | 实验结论 |
| 室温下,将大小相同并打磨光亮的铬片、铝片、铜片分别浸入盛有体积相同、 相同的稀硫酸的试管中。 | 铬片表面产生气泡缓慢,铝片表面产生气泡较快,铜片表面 。 | 猜想 (填序号)成立。 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题
查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题

| 实验事实 | 数据分析及结论 |
| 2.12 g石蜡完全燃烧,得到6.6g CO2和2.88g H2O | 写出计算过程: 结论: 。 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题
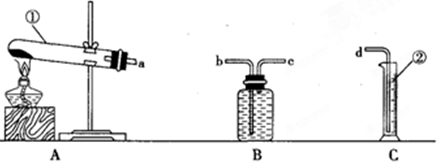
查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题
| 编号 | 盐酸 | NaOH溶液 | △t/℃ |
| 1 | 3.65﹪ | 2.00﹪ | 3.5 |
| 2 | 3.65﹪ | 4.00﹪ | x |
| 3 | 7.30﹪ | 8.00﹪ | 14 |



| 称 量 项 目 | 称 量 时间 | 质量(g) |
| 试样 | | 10.00 |
| 装置+稀硫酸质量 | | 241.20 |
| 装置+稀硫酸质量+试样 | 反应开始后15秒 | 249.20 |
| 装置+稀硫酸质量+试样 | 反应开始后35秒 | 247.00 |
| 装置+稀硫酸质量+试样 | 反应开始后55秒 | 247.00 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题
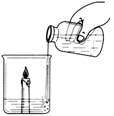
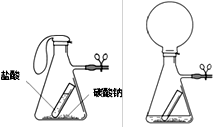

| | 实验操作 | 实验现象 | 结论 |
| 甲 | 取样于试管中,滴加 试液 | 试液变红 | 有盐酸 |
| 乙 | 取样于试管中,逐滴滴加碳酸钠溶液 | |
查看答案和解析>>
科目:初中化学 来源:不详 题型:单选题
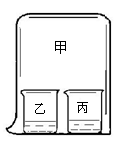
| | 烧杯乙 | 烧杯丙 | 观察到的现象 |
| A. | 浓盐酸 | 紫色石蕊 | 丙中液体慢慢变蓝 |
| B. | 浓盐酸 | 硝酸银 | 丙中产生白色沉淀 |
| C. | 浓硫酸 | 氯化钡 | 丙中产生白色沉淀 |
| D. | 浓氨水 | 无色酚酞 | |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com