
| A. | 只有C、H 两种元素 | B. | 含有C、H、O三种元素 | ||
| C. | C、H、O原子个数比是2:6:3 | D. | C、H原子个数比是1:4 |
分析 根据质量守恒定律可知反应前后原子的种类、数目保持不变来判断化合物元素的种类,且计算各原子的个数比.
解答 解:物质燃烧只生成水和二氧化碳,根据质量守恒定律,则该物质肯定含有碳和氢元素.是否含氧则可根据质量守恒定律由下法确定:
8.8g二氧化碳中碳元素的质量为:8.8g×$\frac{12}{44}$=2.4g;
5.4g水中氢元素的质量为:5.4g×$\frac{2}{18}$=0.6g;
根据质量守恒定律,该物质中碳元素的质量是2.4g,氢元素的质量是0.6g,由此可知,该物质中含有碳元素、氢元素和氧元素,其中氧元素的质量为:4.6g-2.4g-0.6g=1.6g.
由上分析知,物质中碳、氢、氧元素的原子个数比为:$\frac{2.4g}{12}$:$\frac{0.6g}{1}$:$\frac{1.6g}{16}$=2:6:1.
故选B.
点评 熟练掌握质量守恒定律及其实质,并能够运用质量守恒定律及化学式的相关计算求算物质的组成.


 走进文言文系列答案
走进文言文系列答案科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
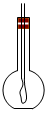 用如图装置做趣味实验:在用胶塞塞紧的烧瓶里充满某种气体(X),烧瓶内导管的一端事先已绑好了一个气球.拔开胶塞,迅速倒入另一种溶液(Y),再立即塞紧胶塞,振荡,此时可以看到气球逐渐膨胀的是( )
用如图装置做趣味实验:在用胶塞塞紧的烧瓶里充满某种气体(X),烧瓶内导管的一端事先已绑好了一个气球.拔开胶塞,迅速倒入另一种溶液(Y),再立即塞紧胶塞,振荡,此时可以看到气球逐渐膨胀的是( )| A. | 二氧化碳(X)、澄清石灰水(Y) | B. | 氧气(X)、水(Y) | ||
| C. | 氮气 (X)、氢氧化钠溶液(Y) | D. | 氢气(X)、硫酸锌溶液(Y ) |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
 一天,实验助手小娟走进实验室,和老师一起检查每个实验桌上的药品、仪器是否齐备,走到某组的时候,看到了一个不和谐的“音符”(如图).
一天,实验助手小娟走进实验室,和老师一起检查每个实验桌上的药品、仪器是否齐备,走到某组的时候,看到了一个不和谐的“音符”(如图).| 探究目的 | 探究步骤 | 预计现象 |
| 除去固体中的碳酸钠 | (1)取少量溶液于试管中, 向其中滴加足量的氯化钙溶液 | 产生白色沉淀 |
| 证明固体中存 在NaOH | (2)向(1)所得溶液中滴加酚酞试液 | 溶液变红 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com