
【题目】同学们对金属模块的内容进行了归纳整理,并找了一些生活中常见的金属制品进行了探究,请你回答下列问题:
(一)图1是有关铁元素的一些信息:
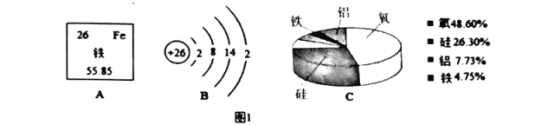
(1)铁的相对原子质量为______,亚铁离子的核外电子数应为_________;
(2)C图应该是铁元素在________(填“海洋中”或“地壳中”)的含量分布图,人体中若缺少铁元素易得________症.
(二)同学们选取了硬币若干(面值分别为一元、五角,一角)和书钉进行了如下探究:
(查阅资料)我国第四套人民币的硬币从1999年开始发行,一元币为钢芯镀镍(Ni),五角币为钢芯镀铜合金,一角币为铝合金或不锈钢,在选择铸造硬币的材料时需要考虑的因素有________(写一条即可).
探究实验一、第一小组同学将一枚五角币放在酒精灯火焰上灼烧片刻,发现表面变黑.
(猜想与假设)
Ⅰ.五角币加热变黑,是因为酒精不完全燃烧产生的_______附着在五角币的表面;
Ⅱ.五角币加热变黑,是因为五角币上的镀铜与_____发生了化学反应.
(实验验证)用洁净的干布擦一擦五角币上的黑色物质,黑色物质不易被擦去;请你另取一枚五角币设计实验证明猜想Ⅰ是不成立的(简述实验操作及现象):__________.
(表达与交流)铜在空气中加热,发生反应的化学反应方程式为________.
探究实验二、第二小组同学探究硬币与酸的反应
分别取一元硬币和一角(铝合金)硬币各一枚,放入小烧杯中,各加入5mL10%的稀盐酸,如图2所示,观察现象:B烧杯中有很少量的气泡产生;A烧杯中开始没有明显变化,过一段时间后开始有气泡产生,产生气泡的速率明显比B中快.试回答下列问题:
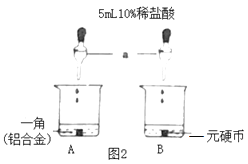
(1)写出![]() 仪器的用途__________.
仪器的用途__________.
(2)A烧杯中开始没有明显变化的原因可能是因为____________.
(3)已知:镍能与稀盐酸反应,生成可溶于水的正二价镍的化合物,并放出氢气,其反应没有铁与酸反应剧烈,镍与稀盐酸反应的化学方程式为______________.
探究实验三、第三小组同学围绕订书钉开展实验研究
(查阅资料)
订书钉主要成分为铁,其表面镀了一种金属,可能是镁、铝、锌、铜中的一种:
(实验研究)
(1)证明书钉主要成分是铁,可采用的物理方法是__________.
(2)为探究书钉表面的金属成分做了如下实验:
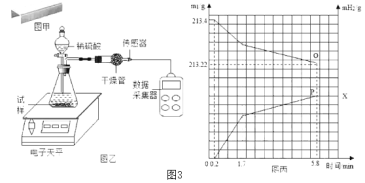
①取一块订书钉(40根钉子)(如图3甲所示),浸入酒精中,一段时间后能从订书钉块上取下一层胶水薄膜
②取上述订书钉块用棉花擦去酒精,并待酒精完全挥发后称量其质量为13.4g
③将其放入图3乙所示装置,并在干燥管口用氢气传感器测量氢气质量,同时记录质量变化(如图3丙所示,ml为天平示数,mH2为传感器示数---即氢气质量,已知干燥管中装的干燥剂用于除去气体中的水分)
④5.8分钟时停止反应,取出装置中剩余订书钉,洗涤、干燥、称量,剩余订书钉质量为7.8g
(分析与结论)
(1)订书钉表面涂胶水的目的主要是_________.
(2)请结合图丙分析:
①图丙中P点纵坐标X的值为________________.
②参加反应的金属的总质量为_______g.
③根据丙图可知订书钉表面镀的金属应该比铁________(填“活泼”或“不活泼”).
④请根据实验数据分析订书钉表面镀的金属应该是镁、铝、锌、铜中的___________.
【答案】26 24 地壳中 贫血 金属的硬度(或金属耐腐蚀性或金属的成本)(合理即可) 炭黑 氧气 取一块铜片放入小试管中并塞上橡皮塞,然后用酒精灯加热,试管中铜片变黑。 2Cu + O2 ![]() 2CuO 吸取和滴加少量液体 铝表面有一层致密的氧化膜,盐酸先与氧化膜反应,阻碍了铝与稀盐酸反应 Ni+2HCl=NiCl2+H2↑ 用磁铁吸引订书钉,发现订书钉能被吸引 防止订书钉生锈 0.18g 5.6g 活泼 Zn(或锌)
2CuO 吸取和滴加少量液体 铝表面有一层致密的氧化膜,盐酸先与氧化膜反应,阻碍了铝与稀盐酸反应 Ni+2HCl=NiCl2+H2↑ 用磁铁吸引订书钉,发现订书钉能被吸引 防止订书钉生锈 0.18g 5.6g 活泼 Zn(或锌)
【解析】
(一):
(1)根据元素周期表提供的信息可知,左上角的数字表示原子序数,铁的原子序数26;在原子中,原子序数=质子数=核外电子数,铁原子核外有26个电子,形成亚铁离子时失去了2个电子,亚铁离子还有24个电子;
(2)根据图示可知,铁的含量为第四位,在地壳中铁元素含量是第四位,C图应该是铁元素在地壳中的含量分布图,缺铁易患贫血;
(二):
在选择铸造硬币的材料时需要考虑的因素有:金属的硬度、金属耐腐蚀性、金属的成本等;
探究实验一:
Ⅰ.酒精不完全燃烧产生会产炭黑。五角币加热变黑,是因为酒精不完全燃烧产生的炭黑附着在五角币的表面;
Ⅱ.铜与氧气加热反应生成黑色的氧化铜。五角币加热变黑,是因为五角币上的镀铜与氧气发生了化学反应;
实验验证:用洁净的干布擦一擦五角币上的黑色物质,黑色物质不易被擦去;若证明猜想Ⅰ不成立,说明黑色物质不是酒精不完全燃烧产生的炭黑附着在五角币的表面,可将五角币加热时,不与酒精灯的火焰接触,观察是否有黑色物质生成。具体操作及实验现象为:取一块铜片放入小试管中并塞上橡皮塞,然后用酒精灯加热,试管中铜片变黑;
表达与交流:铜在空气中加热生成氧化铜,发生反应的化学反应方程式为:2Cu + O2 ![]() 2CuO;
2CuO;
探究实验二:
(1)a是胶头滴管,用途是吸取和滴加少量液体;
(2)A烧杯中开始没有明显变化的原因可能是因为铝表面有一层致密的氧化膜,盐酸先与氧化膜反应,阻碍了铝与稀盐酸反应;
(3)镍能与稀盐酸反应,生成可溶于水的正二价镍的化合物,并放出氢气,镍与稀盐酸反应的化学方程式为:Ni+2HCl=NiCl2+H2↑;
探究实验三:
实验研究:(1)铁能被磁铁吸引。证明订书钉主要成分是铁,可采用的物理方法是用磁铁吸引订书钉,发现订书钉能被吸引;
分析与结论:(1)铁在潮湿的空气中会发生锈蚀,订书钉表面涂胶水能隔绝氧气和水,目的主要是防止订书钉生锈;
(2)①金属与酸反应生成的氢气全部逸出反应容器,样品与酸反应减少的质量=213.4g-213.22g=0.18g,所以反应过程中产生氢气的质量为0.18g,图丙中P点纵坐标表示生成氢气的质量,所以X的值是0.18g;
②反应过程中固体减少的质量=参加反应的金属的总质量=13.4g-7.8g=5.6g
③根据丙图可知,0→0.2分钟不产生氢气,可能是订书钉表面有少量金属氧化物会先与酸发生反应,0.2→1.7分钟反应速度较快,1.7分钟后反应的速度较慢,订书钉中至少有两种金属产生氢气产生,订书钉主要成分为铁,其表面镀了一种金属,可能是镁、铝、锌、铜中的一种,铜不能与硫酸反应产生氢气,书钉表面镀的金属应该是镁、铝、锌中的一种,镁、铝、锌都比铁活泼,所以订书钉表面镀的金属应该比铁活泼;
④根据化学方程式Fe + H2SO4 = FeSO4 + H2↑可知,每56份质量的铁会生成2份质量的氢气;根据化学方程式Mg + H2SO4 = MgSO4 + H2↑可知,每24份质量的镁会生成2份质量的氢气;根据化学方程式2Al + 3H2SO4 = Al2(SO4)3 + 3H2↑可知,每18份质量的铝会生成2份质量的氢气;根据化学方程式Zn+ H2SO4 =ZnSO4 + H2↑可知,每65份质量的锌会生成2份质量的氢气,5.6g的订书钉与酸反应生成0.18g的氢气。所以相同质量的订书钉表面镀的金属与足量酸反应产生的氢气比铁少,该金属可能是Zn。


科目:初中化学 来源: 题型:
【题目】盐通高铁的建成将进一步推动我市经济的发展,在修建铁路的土石方爆破中要用到黑火药,黑火药爆炸时发生反应的化学方程式是2KNO3+3C+S![]() K2S+3CO2↑+X↑,根据以上信息,回答下列问题:
K2S+3CO2↑+X↑,根据以上信息,回答下列问题:
(1)X的化学式是_________。
(2)KNO3中的阴离子是 ________ (填离子符号)。
(3)K2S中硫元素的化合价为 ________ (填序号)。
A.0 B.-2 C.+6 D.+2
(4)黑火药属于_________ (“混合物”或“纯净物”)。
(5)KNO3属于 ________ (填序号)。
A.单质B.化合物C.氧化物D.纯净物
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图所示为实验室中常见的气体制备和收集装置。
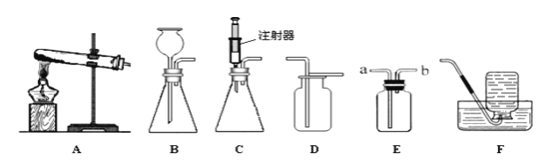
(1)实验室用加热氯酸钾和二氧化锰的混合物制取氧气,应选用发生装置_______(填字母序号),反应的文字表达式为___________________。试管口略向下倾斜的原因是________ 。实验结束后,应先______________,再 ___________,防止_______________。
(2)若用F装置收集氧气,___________ 开始收集,_______________证明收集满了。若用装置D收集氧气,验满的方法是_______________________。
(3)实验室用过氧化氢溶液和二氧化锰制取氧气,若选用B做发生装置,加入药品前应先_____________。具体做法是__________________。若选用C做发生装置,你认为选用C的优点是_________________。
(4)欲使用装置E用排空气法收集氧气,则气体应从______(填“a”或“b”)端通入;欲使用装置E用排水法收集氧气,先将瓶中装满水,再将气体从______(填“a”或“b”)端通入。
(5)已知一氧化氮气体难溶于水,在空气中容易与氧气发生反应,则收集一氧化氮气体时应选用图中装置________(填字母序号)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】水是人类赖以生存的物质之一,人们的生活需要干净的水。试回答下列问题:
(1)下列净水方法:①静置沉淀;②蒸馏;③吸附沉淀;④过滤,净水程度由高到低的顺序是______。
A.①②③④ B.①③④② C.②④③① D.④③②①
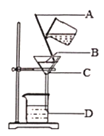
(2)如图为过滤装置。写出下列仪器、用品的名称:A______(作用:______),C______;某同学用如图的装置进行过滤操作,实验后发现滤液仍浑浊,请你写出可能的两点原因:
①_______,②______;试举出生活中利用过滤原理的实例:______。
(3)净水时,常用______(填序号,下同)作为吸附剂来除去水中的色素和异味,净化后水变澄清:用______来区分净化后的水是软水还是硬水。
①明矾 ②食盐水 ③活性炭 ④肥皂水 ⑤漂白粉[主要成分是![]() ]
]
(4)生活中常用______方法使硬水转化成软水。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】图1是实验室制取气体的常用装置(部分固定装置已略去):
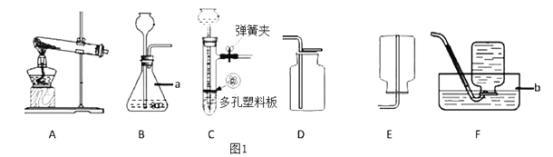
(1)写出图1中标号仪器的名称:a:_________b:_________
(2)选择装置A和F用加热高锰酸钾的方法制取氧气:
①装置A和F的玻璃导管之间要用_________连接(填实验用品);
②为了防止高锰酸钾粉未进入导管,应采取的措施是___________;
③装置A中发生反应的化学方程式为__________,在反应中锰元素的化合价发生的变化是______;
(3)B或C装置均可用作制取![]() 的发生装置,发生反应的化学方程式为___________,C装置的优点是能控制反应的发生和停止,请简述使C装置中反应停止的方法及原理: ___________.
的发生装置,发生反应的化学方程式为___________,C装置的优点是能控制反应的发生和停止,请简述使C装置中反应停止的方法及原理: ___________.
(4)加热氯化铵和熟石灰固体混合物可制取氨气(![]() ),氨气密度比空气小,极易溶于水:
),氨气密度比空气小,极易溶于水:
①制取氨气应选用的一套装置是___________(填图1中字母代号);
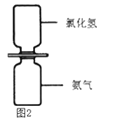
②将盛有氯化氢气体和制得的氨气的两个集气瓶(如图2所示)之间的玻璃片抽掉后会有大量白烟(氯化铵)产生,试结合微粒观点解释产生白烟的原因___________.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】表示下列反应的化学方程式中,完全正确的是
A. 细铁丝在氧气中燃烧:4Fe+3O2═2Fe2O3
B. 加热氯酸钾和二氧化锰的混合物制氧气:KClO3═KCl+O2 ↑
C. 水在直流电作用下分解: 2H2O![]() 2H2↑+ O2↑
2H2↑+ O2↑
D. 甲烷(CH4)在空气中燃烧生成二氧化碳和水:CH4↑+2O2↑![]() 2H2O+CO2↑
2H2O+CO2↑
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】A、B、C、D是初中化学常见的纯净物,B是绿色植物光合作用时吸收的物质,A为单质,B、C、D均为氧化物。其转化关系如右图所示(图中“—”表示相连的两种物质能发生反应, “→”表示一种物质转化成另一种物质,部分反应物、生成物及反应条件已省略)。
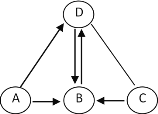
(1)则A的化学式为_________;B的化学式为________。
(2)写出由C与D反应的化学方程式_____________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】关于化学方程式CH4+2O2![]() CO2+2H2O的描述正确的是( )
CO2+2H2O的描述正确的是( )
A. 甲烷加氧气在点燃的条件下,反应生成二氧化碳和水
B. 1个甲烷和2个氧气在点燃的条件下,生成1个二氧化碳和2个水
C. 1个甲烷分子和2个氧气分子在点燃的条件下,生成1个二氧化碳分子和2个水分子
D. 1g甲烷和2g氧气在点燃的条件下,生成1g二氧化碳和2g水
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在用白磷(白磷与红磷组成相同,着火点为40℃)探究质量守恒定律的实验中,晓涵同学将橡皮塞上的细玻璃管下端放到酒精灯火焰上灼烧至红热后,迅速用橡皮塞将锥形瓶塞紧,并引燃白磷,实验过程如下图所示。请回答下列问题:
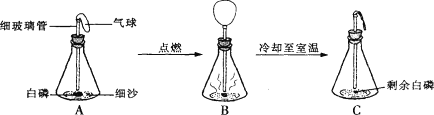
(1)此实验能否不用气球,改为直接用橡皮塞使锥形瓶密封?且说明理由____________
(2)实验中观察到气球先变大后变小,用理化知识解释产生此现象的原因是____________
(3)该同学联想到以前测定氧气体积分数时也用到红磷,且当时红磷必须过量,请解释原因。________。经过分析该同学认为上述探究质量守恒定律的实验中红磷也应过量,你认为她的观点正确吗?并加以解释____________________
(4)上述探究质量守恒定律的实验后,该同学为了验证锥形瓶内是否还有氧气剩余,用如下方法:打开瓶塞,用燃着的木条伸入锥形瓶,发现木条继续燃烧,说明瓶内还有少量氧气剩余。请你评价其实验方法正确与否,并解释:____________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com