
| ���� | Na2SO4 | Na2CO3 | NaHCO3 |
| �ܽ��/g | 19.5 | 21.5 | 9.6 |
| ʵ �� �� �� | ʵ �� �� �� | ʵ �� �� �� |
| ȡ������Һ���Թ��У���ϡ���� | ��Һ�����ݲ��� | ����Һ��______��Һ |
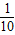 ������������������Һ��Ӧ���������ܲ������ٿ˳�����
������������������Һ��Ӧ���������ܲ������ٿ˳�����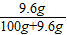 ×100%=9.6%�ʴ�Ϊ��NaHCO3��9.6%
×100%=9.6%�ʴ�Ϊ��NaHCO3��9.6%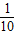 x
x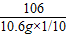 =
=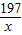



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
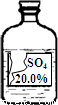
 Сǿͬѧ�ڻ�ѧʵ���ҷ���һƿʢ����ɫ��Һ���Լ�ƿ�����ǩ����������ͼ��ʾ������ʦ����������ƿ�Լ����������ᡢ�����ơ�����þ��Һ�е�һ�֣�Сǿͬѧͨ���������ϵ�֪�����������������ʵ��ܽ�����±���
Сǿͬѧ�ڻ�ѧʵ���ҷ���һƿʢ����ɫ��Һ���Լ�ƿ�����ǩ����������ͼ��ʾ������ʦ����������ƿ�Լ����������ᡢ�����ơ�����þ��Һ�е�һ�֣�Сǿͬѧͨ���������ϵ�֪�����������������ʵ��ܽ�����±���| �� �� | H2SO4 | Na2SO4 | MgSO4 |
| �ܽ��/g | ��ˮ����Ȼ��� | 19.0 | 39.0 |
| ʵ�鲽�� | ʵ������ | ʵ����� |
| Сǿ�IJ�������ȷ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ���� | Na2SO4 | Na2CO3 | NaHCO3 |
| �ܽ��/g | 19.5 | 21.5 | 9.6 |
| ʵ �� �� �� | ʵ �� �� �� | ʵ �� �� �� |
| ȡ������Һ���Թ��У���ϡ���� | ��Һ�����ݲ��� | ����Һ�� Na2CO3 Na2CO3 ��Һ |
| 1 |
| 10 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ʡ�п����� ���ͣ�ʵ����


�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2012��ɽ��ʡ������������ʵ����ѧ�п���ѧģ���Ծ��������棩 ���ͣ������
| ���� | Na2SO4 | Na2CO3 | NaHCO3 |
| �ܽ��/g | 19.5 | 21.5 | 9.6 |
| ʵ �� �� �� | ʵ �� �� �� | ʵ �� �� �� |
| ȡ������Һ���Թ��У���ϡ���� | ��Һ�����ݲ��� | ����Һ��______��Һ |
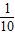 ������������������Һ��Ӧ���������ܲ������ٿ˳�����
������������������Һ��Ӧ���������ܲ������ٿ˳������鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2012�����ʡ���������п���ѧģ���Ծ��������������棩 ���ͣ������
| �� �� | H2SO4 | Na2SO4 | MgSO4 |
| �ܽ��/g | ��ˮ����Ȼ��� | 19.0 | 39.0 |
| ʵ�鲽�� | ʵ������ | ʵ����� |
| Сǿ�IJ�������ȷ�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com