
| Ćū³Ę | æÕĘųÖŠĢå»ż ·ÖŹż£Ø%£© |
±ź×¼×“æöĻĀĆÜ¶Č£Øg?m-1£© | ·Šµć£Ø”ę£© | Ķس£×“æöĻĀ£ŗ1Ģå»ż Ė®ÖŠČܽāµÄĢå»żŹż |
| µŖĘų | 78 | 1.2505 | -195.8 | 0.02 |
| ŃõĘų | 21 | 1.429 | -183.0 | 0.03 |
| ¶žŃõ»ÆĢ¼ | 0.03 | 1.977 | -78.44 | 1.00 |


 ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø
ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŌĶĮĄķ½ā
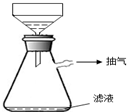 ĮņĖįĶŹĒÉś²ś”¢Éś»īÖŠ³£¼ūµÄĪļÖŹ£¬ĻĀĆęŹĒÄ³Ń§Ļ°Š”×éÕ¹æŖµÄĢ½¾æŹµĀ¼£ŗ
ĮņĖįĶŹĒÉś²ś”¢Éś»īÖŠ³£¼ūµÄĪļÖŹ£¬ĻĀĆęŹĒÄ³Ń§Ļ°Š”×éÕ¹æŖµÄĢ½¾æŹµĀ¼£ŗ
| ||
| ||
| Alʬ£ØĪ““ņÄ„£© | Alʬ£Ø“ņÄ„£© | |
| CuSO4ČÜŅŗ £Ø5%£¬5mL£© |
ĪŽ±ä»Æ£¬ŹżŠ”Ź±ŗóĀĮʬÉĻø½ÓŠ¼«ÉŁĘųÅŻ£¬¼øŗõĪŽŗģÉ«ĪļÖŹ | ¼«ÉŁĘųÅŻ£¬ø½×ż«ÉŁŗģÉ«ĪļÖŹ£¬³ÖŠų½Ļ³¤Ź±¼ä |
| CuSO4ČÜŅŗ £Ø10%£¬5mL£© |
ĪŽ±ä»Æ£¬ŹżŠ”Ź±ŗóĀĮʬø½ÓŠÉŌ¶ąĘųÅŻ£¬½öÓŠ¼«ÉŁŗģÉ«°ßµć | ÉŌ¶ąĘųÅŻ£¬ø½×ż«ÉŁ£Ø¶ąÓŚ5%£©ŗģÉ«ĪļÖŹ£¬³ÖŠų½Ļ³¤Ź±¼ä |
| CuCl2ČÜŅŗ £Ø5%£¬5mL£© |
¶ąĮæĘųÅŻ£¬ŃøĖŁ³öĻÖŗģÉ«ĪļÖŹ£¬ŗÜæģČÜŅŗ±ä³ÉĪŽÉ«£¬ĒŅĪĀ¶ČÉżøß | øü¶ąĮæĘųÅŻ£¬ŃøĖŁ³öĻÖŗģÉ«ĪļÖŹ£¬ŗÜæģČÜŅŗ±ä³ÉĪŽÉ«£¬ĒŅĪĀ¶ČÉżøß |
| ||
| ||
| ||
| ||
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
| ŹµŃé ŠņŗÅ |
¹żŃõ»ÆĒāČÜŅŗÅضČ/% | ¹żŃõ»ÆĒāČÜŅŗĢå»ż/ml | ĪĀ¶Č/”ę | ¶žŃõ»ÆĆĢµÄÓĆĮæ/g | ŹÕ¼ÆŃõĘųµÄĢå»ż/ml | ·“Ó¦ĖłŠčµÄŹ±¼ä/s |
| ¢Ł | 5 | 1 | 20 | 0.1 | 4 | 16.75 |
| ¢Ś | 15 | 1 | 20 | 0.1 | 4 | 6.04 |
| ¢Ū | 30 | 5 | 35 | --------------- | 2 | 49.21 |
| ¢Ü | 30 | 5 | 55 | --------------- | 2 | 10.76 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
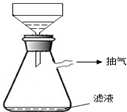 ĮņĖįĶŹĒÉś²ś”¢Éś»īÖŠ³£¼ūµÄĪļÖŹ£¬ĻĀĆęŹĒÄ³Ń§Ļ°Š”×éÕ¹æŖµÄĢ½¾æŹµĀ¼£ŗ
ĮņĖįĶŹĒÉś²ś”¢Éś»īÖŠ³£¼ūµÄĪļÖŹ£¬ĻĀĆęŹĒÄ³Ń§Ļ°Š”×éÕ¹æŖµÄĢ½¾æŹµĀ¼£ŗ| Alʬ£ØĪ““ņÄ„£© | Alʬ£Ø“ņÄ„£© | |
| CuSO4ČÜŅŗ £Ø5%£¬5mL£© | ĪŽ±ä»Æ£¬ŹżŠ”Ź±ŗóĀĮʬÉĻø½ÓŠ¼«ÉŁĘųÅŻ£¬¼øŗõĪŽŗģÉ«ĪļÖŹ | ¼«ÉŁĘųÅŻ£¬ø½×ż«ÉŁŗģÉ«ĪļÖŹ£¬³ÖŠų½Ļ³¤Ź±¼ä |
| CuSO4ČÜŅŗ £Ø10%£¬5mL£© | ĪŽ±ä»Æ£¬ŹżŠ”Ź±ŗóĀĮʬø½ÓŠÉŌ¶ąĘųÅŻ£¬½öÓŠ¼«ÉŁŗģÉ«°ßµć | ÉŌ¶ąĘųÅŻ£¬ø½×ż«ÉŁ£Ø¶ąÓŚ5%£©ŗģÉ«ĪļÖŹ£¬³ÖŠų½Ļ³¤Ź±¼ä |
| CuCl2ČÜŅŗ £Ø5%£¬5mL£© | ¶ąĮæĘųÅŻ£¬ŃøĖŁ³öĻÖŗģÉ«ĪļÖŹ£¬ŗÜæģČÜŅŗ±ä³ÉĪŽÉ«£¬ĒŅĪĀ¶ČÉżøß | øü¶ąĮæĘųÅŻ£¬ŃøĖŁ³öĻÖŗģÉ«ĪļÖŹ£¬ŗÜæģČÜŅŗ±ä³ÉĪŽÉ«£¬ĒŅĪĀ¶ČÉżøß |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ2011-2012ѧğ°²»ÕŹ”°ö²ŗŹŠŠĀ³ĒŹµŃéѧŠ£¾ÅÄź¼¶£ØÉĻ£©ŌĀæ¼»ÆѧŹŌ¾ķ£ØµŚŅ»”¢¶žµ„ŌŖ£©£Ø½āĪö°ę£© ĢāŠĶ£ŗ½ā“šĢā
| ŹµŃé ŠņŗÅ | ¹żŃõ»ÆĒāČÜŅŗÅضČ/% | ¹żŃõ»ÆĒāČÜŅŗĢå»ż/ml | ĪĀ¶Č/”ę | ¶žŃõ»ÆĆĢµÄÓĆĮæ/g | ŹÕ¼ÆŃõĘųµÄĢå»ż/ml | ·“Ó¦ĖłŠčµÄŹ±¼ä/s |
| ¢Ł | 5 | 1 | 20 | 0.1 | 4 | 16.75 |
| ¢Ś | 15 | 1 | 20 | 0.1 | 4 | 6.04 |
| ¢Ū | 30 | 5 | 35 | --------------- | 2 | 49.21 |
| ¢Ü | 30 | 5 | 55 | --------------- | 2 | 10.76 |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com