
 甲、乙两种固体物质的溶解度曲线如图所示,下列说法正确的是( )
甲、乙两种固体物质的溶解度曲线如图所示,下列说法正确的是( )| A. | t2℃时,向100g甲中加入100g水后形成溶液的质量为200g | |
| B. | t1℃时,甲、乙两种物质的溶解度相等 | |
| C. | 甲的溶解度比乙大 | |
| D. | 将t2℃时甲、乙的饱和溶液分别降到t1℃时,两溶液的溶质质量分数相等 |
分析 根据固体物质的溶解度曲线可以:①某物质在某温度下的溶解度,②判断物质的溶解度随温度变化的变化情况,③比较不同物质在同一温度下的溶解度的大小,④判断通过降温还是升温的方法是晶体析出,据此解答.
解答 解:A、t2℃时,甲的溶解度是80g,向100g甲中加入100g水后,只能溶解80g,形成溶液的质量为100g+80g=180g,错误;
B、t1℃时,甲、乙两种物质的溶解度相等,正确;
C、在同一温度下比较不同的物质的溶解度的大小,没提温度,不能比较,错误;
D、将t2℃时甲、乙的饱和溶液分别降到t1℃时,甲的溶解度减小,有晶体析出,溶质质量分数是t1℃时的饱和溶液的溶质质量分数,而乙的溶解度随温度的降低而增大,故溶液组成不变,溶质质量分数是t2℃时的溶质质量分数,根据图象可以看出,两溶液的溶质质量分数是甲的大于乙,错误;
故选B.
点评 本题难度不是很大,主要考查了固体溶解度曲线的意义及根据溶解度曲线解决相关的问题,培养学生应用知识解决问题的能力.


 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案 名校提分一卷通系列答案
名校提分一卷通系列答案科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
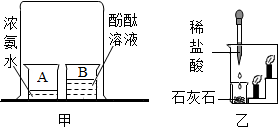 实验是进行科学探究的重要方式,请根据下图回答有关问题.
实验是进行科学探究的重要方式,请根据下图回答有关问题.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
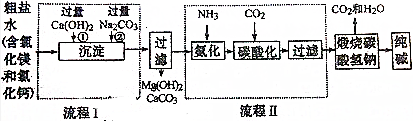
| A. | 用食盐制纯碱需要含碳、氧元素的物质 | |
| B. | (1)中析出晶体后剩余溶液只有一种溶质 | |
| C. | 氨盐水比食盐水更易吸收二氧化碳 | |
| D. | 碳酸氢钠比碳酸钠受热更易分解 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验步骤 | 实验现象 | 结论 | |
| 小王 | 用pH试纸测溶液的pH | 溶液的pH>7 | 说明氢氧化钠溶液没有变质 |
| 小李 | 取少量溶液于试管中,加入适量氯化钡溶液 | A | 说明氢氧化钠溶液已经变质 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
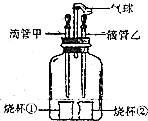 在一次实验创新比赛中,小亮设计了如图所示装置,完成了多个简单实验,该装置具有药品用量少,实验现象明显,尾气不外逸等优点.
在一次实验创新比赛中,小亮设计了如图所示装置,完成了多个简单实验,该装置具有药品用量少,实验现象明显,尾气不外逸等优点.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
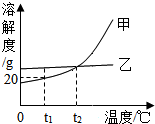 甲、乙两种不含结晶水的固体物质的溶解度曲线如图,下列说法中正确的是( )
甲、乙两种不含结晶水的固体物质的溶解度曲线如图,下列说法中正确的是( )| A. | 甲的溶解度比乙大 | |
| B. | t2℃时,甲、乙的两种溶液中溶质的质量分数相等 | |
| C. | t1℃时,将50g水加入15g甲物质中,可得到65g溶液 | |
| D. | 要使接近饱和的乙溶液转化为饱和溶液,可采用蒸发溶剂的方法 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 加入明矾使小颗粒凝聚 | B. | 通入氯气杀菌消毒 | ||
| C. | 通过沙滤装置除去可溶性杂质 | D. | 通过活性炭吸附部分有害物质 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com