
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
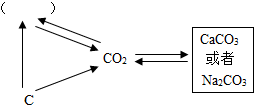 构建模型和构建知识网络是化学学习中重要的学习方法,碳元素是构成物质种类最多的一种元素,请结合如图回答下列问题:
构建模型和构建知识网络是化学学习中重要的学习方法,碳元素是构成物质种类最多的一种元素,请结合如图回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:填空题
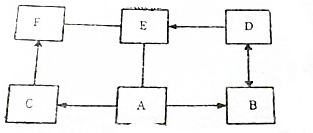 A→F是初中化学常见的六种不同物质,它们相互关系如图(“→”表示物质间的转化关系,“-”表示两端的物质能发生化学反应),已知A是胃液中含有的酸,B是最轻的气体,C、D都是氧化物,E可以改良酸性土壤,回答下列问题:
A→F是初中化学常见的六种不同物质,它们相互关系如图(“→”表示物质间的转化关系,“-”表示两端的物质能发生化学反应),已知A是胃液中含有的酸,B是最轻的气体,C、D都是氧化物,E可以改良酸性土壤,回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
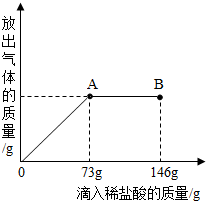 已知 Na2CO3的水溶液呈碱性,在一烧杯中盛有20.4g Na2CO3和NaCl组成的固体混合物.向其中逐渐滴加溶质质分数为10%的稀盐酸.放出气体的总质量与所滴入稀盐酸的质量关系曲线如图所示,请根据题意回答问题:
已知 Na2CO3的水溶液呈碱性,在一烧杯中盛有20.4g Na2CO3和NaCl组成的固体混合物.向其中逐渐滴加溶质质分数为10%的稀盐酸.放出气体的总质量与所滴入稀盐酸的质量关系曲线如图所示,请根据题意回答问题:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 奥司他韦属于氧化物 | |
| B. | 奥司他韦中氢元素的质量分数约为8.97% | |
| C. | 奥司他韦由碳、氢、氮、氧四种原子构成 | |
| D. | 奥司他韦中碳、氢、氮、氧元素质量比为8:14:1:2 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
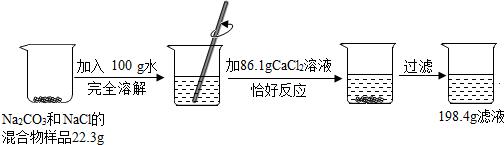
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
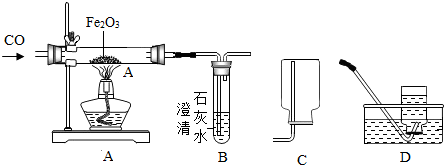
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com