

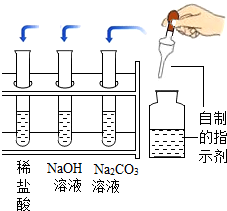
 | 选择的溶液 | 加西红柿汁(黄色) | 加红萝卜汁(红色) | 加茄子汁 (紫色) | 加杜鹃花汁(紫色) |
| 稀盐酸 | 不变色 | 浅红色 | 桃红色 | 浅红色 | |
| 氢氧化钠 | 不变色 | 黄绿色 | 亮黄色 | 变黄色 | |
| 碳酸钠 | 不变色 | 黄绿色 | 亮黄色 | 变黄色 |
| 自制指示剂 | pH=1~4 | pH=5~6 | pH=7 | pH=8~9 | pH=10~12 | pH=13~14 |
| 杜鹃花汁(紫红) | 浅红 | 微红 | 无色 | 浅黄色 | 浅绿色 | 黄色逐渐加深 |
| 茄子皮汁(紫色) | 红色渐浅 | 浅褐色 | 浅褐色 | 浅褐色 | 浅黄绿色 | 亮黄色 |
| 红萝卜汁(红色) | 浅红 | 无色 | 无色 | 无色 | 无色 | 黄绿色 |
分析 (1)根据实验室常用仪器解答;
(2)根据物质在在酒精中的溶解度比在水中大或不易溶于水易溶于酒精等解答;
(3)根据四种汁液在稀酸和稀碱中西红柿汁颜色不变,因此不可做指示剂解答;
(4)根据表中数据及颜色变化分析解答;
(5)根据表中数据及颜色变化分析解答;
(6)根据已有的知识进行分析,酸碱盐之间两两反应需能产生气体、沉淀或水解答;
(7)pH小于7的溶液呈酸性;碳酸盐遇酸化气,据此解答.
解答 解:
(1)根据实验室常用仪器可知:研钵;
(2)用酒精浸泡不用水浸泡的原因可能是指示剂中的有效成分具有在酒精中的溶解度比在水中大或不易溶于水易溶于酒精等的性质;
(3)四种汁液在稀酸和稀碱中西红柿汁颜色不变,因此不可做指示剂;
(4)根据表中数据及颜色变化可知:杜鹃花汁在酸和碱中会呈现不同的颜色,故小冰的结论正确;
(5)根据表中数据及颜色变化可知:红萝卜汁只能检验强酸性或强碱性的溶液或红萝卜汁只能在强酸性或强碱性的溶液中才能变色或在pH值为5~12时,溶液都不变色或无法检验pH值为5~12时溶液的酸碱性;
(6)氢氧化钠先和稀盐酸反应,生成氯化钠和水,碳酸钠和稀盐酸反应,生成氯化钠、水和二氧化碳,用pH试纸测试溶液显碱性,溶液中一定存在的溶质
是:氯化钠和碳酸钠,可能有氢氧化钠;
(7)为确认废液中可能存在的物质是否存在,她取少量废液样品,向其中加入过量的氯化钙或过量的硝酸钙或过量的氯化钡或过量的硝酸钡,再用pH试纸测试,确定了废液的成分.
答案:
(1)研钵;
(2)在酒精中的溶解度比在水中大或不易溶于水易溶于酒精等;
(3)西红柿汁;
(4)小冰;
(5)红萝卜汁只能检验强酸性或强碱性的溶液;
(6)氯化钠和碳酸钠;
(7)过量的氯化钙或过量的硝酸钙或过量的氯化钡或过量的硝酸钡.
点评 此题是对指示剂知识的考查,解题的关键是对题干中提供的信息进行有效地归纳整理,然后再结合所学的指示剂知识解决即可.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:解答题
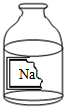 某校兴趣小组同学准备进行常见酸、碱、盐的性质实验时,发现实验台上摆放的药品中(如图),有一装溶液的试剂未盖瓶盖且标签破损,于是决定对这瓶溶液进行实验探究:
某校兴趣小组同学准备进行常见酸、碱、盐的性质实验时,发现实验台上摆放的药品中(如图),有一装溶液的试剂未盖瓶盖且标签破损,于是决定对这瓶溶液进行实验探究:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 酒精做燃料 C2H5OH+3O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+3H2O 氧化反应 | |
| B. | 电解水制取氢气 2H2O$\frac{\underline{\;电解\;}}{\;}$2H2+O2 分解反应 | |
| C. | 制取少量硫酸铜溶液 H2SO4+CuCl2═CuSO4+2HCl 复分解反应 | |
| D. | 碳还原氧化铜 2CuO+C$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑ 置换反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 1:1:1 | B. | 1:2:3 | C. | 6:3:2 | D. | 117:222:267 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 如图A、B、C、D是初中化学常见的不同类别的化合物,其中A为黑色固体.图中“-”表示两物质能相互反应.“→”表示两物质间的转化.
如图A、B、C、D是初中化学常见的不同类别的化合物,其中A为黑色固体.图中“-”表示两物质能相互反应.“→”表示两物质间的转化.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | KOH、KCl、H2SO4 | B. | H2SO4、KOH、KCl | C. | KOH、H2SO4、KCl | D. | KCl、KOH、H2SO4 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 酸、碱和盐是初中阶段化学学习的重要内容,根据它们相互间的反应现象进行合理推断更是同学们必须具备的综合能力,飞飞同学的具体实验操作流程示意图如下:
酸、碱和盐是初中阶段化学学习的重要内容,根据它们相互间的反应现象进行合理推断更是同学们必须具备的综合能力,飞飞同学的具体实验操作流程示意图如下:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com