
分析 (1)根据pH值来决定酸碱的反应情况从而决定溶液中的溶质成分;
(2)根据恰好反应时消耗的盐酸质量来计算氢氧化钠的质量即可解答.
解答 解:(1)当溶液的pH大于7时,说明溶液显碱性,即氢氧化钠有剩余,所以溶液中的溶质是生成的氯化钠和剩余的氢氧化钠;
(2)设20.0g氢氧化钠溶液中溶质的质量为x,
HCl+NaOH=NaCl+H2O
36.5 40
20g×7.3% x
$\frac{36.5}{20g×7.3%}$=$\frac{40}{x}$
x=1.6g
氢氧化钠溶液中溶质的质量分数:$\frac{1.6g}{40g}$×100%=4%.
答:所测氢氧化钠溶液中溶质的质量分数是4%.
故答案为:(1)NaCl、NaOH;
(2)所测氢氧化钠溶液中溶质的质量分数是4%.
点评 本题主要考查了学生根据化学方程式进行简单计算的能力,比较简单,关键是解题步骤要规范.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:解答题
 碳酸钙是钙片的主要原料.右图是某钙片说明书上的部分内容.兴趣小组的同学为了测定该钙片说明书上有关碳酸钙含量标注是否属实,进行了如下实验:取出4片片剂,研碎后放入烧杯中,加入过量的稀盐酸,同时测量6分钟(min)内生成CO2质量,测量数据如下表:(假定钙片中其它成分不与盐酸反应)
碳酸钙是钙片的主要原料.右图是某钙片说明书上的部分内容.兴趣小组的同学为了测定该钙片说明书上有关碳酸钙含量标注是否属实,进行了如下实验:取出4片片剂,研碎后放入烧杯中,加入过量的稀盐酸,同时测量6分钟(min)内生成CO2质量,测量数据如下表:(假定钙片中其它成分不与盐酸反应)| 时间/min | 1 | 2 | 3 | 4 | 5 | 6 |
| 生成CO2的质量/g | 1.0 | 1.8 | 2.0 | 2.2 | M | 2.2 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 打开盛有浓盐酸和浓硫酸的试剂瓶瓶塞,在瓶口都有白雾 | |
| B. | 长期敞口露置在空气中的浓盐酸,其溶质质量分数会减小 | |
| C. | 浓盐酸和浓硫酸都可以作为干燥剂 | |
| D. | 稀释浓硫酸时,将水倒入浓硫酸中 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
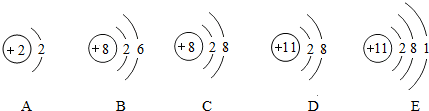
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 22.8% | B. | 78% | C. | 9.2% | D. | 10.9% |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com