
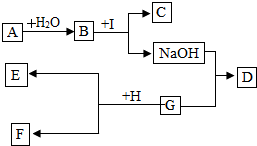
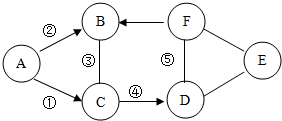
 如图是初中化学中常见的物质之间的转换 关系,其中A为常用的食品干燥剂,C为白色沉淀,D 为蓝色沉淀,E为红色的固体单质.请你回答问题:
如图是初中化学中常见的物质之间的转换 关系,其中A为常用的食品干燥剂,C为白色沉淀,D 为蓝色沉淀,E为红色的固体单质.请你回答问题:分析 根据A为常用的食品干燥剂,所以A是氧化钙,水和氧化钙反应生成氢氧化钙,所以B是氢氧化钙,氢氧化钙和I反应生成白色沉淀D和氢氧化钠,依据复分解反应原理可知,I是碳酸钠,C是碳酸钙,D为蓝色沉淀,E为红色的固体单质,氢氧化钠和G反应会生成蓝色沉淀,所以D是氢氧化铜沉淀,G可以是氯化铜,H是铁,铁和硫氯化铜反应生成氯化亚铁和铜,所以E是铜,F是氯化亚铁,然后将推出的物质进行验证即可.
解答 解:(1)A为常用的食品干燥剂,所以A是氧化钙,水和氧化钙反应生成氢氧化钙,所以B是氢氧化钙,氢氧化钙和I反应生成白色沉淀D和氢氧化钠,依据复分解反应原理可知,I是碳酸钠,C是碳酸钙,D为蓝色沉淀,E为红色的固体单质,氢氧化钠和G反应会生成蓝色沉淀,所以D是氢氧化铜沉淀,G可以是氯化铜,H是铁,铁和硫氯化铜反应生成氯化亚铁和铜,所以E是铜,F是氯化亚铁,经过验证,推导正确,所以A是CaO,D是Cu(OH)2;
(2)B和I的反应是碳酸钠和氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,化学方程式为:Na2CO3+Ca(OH)2=CaCO3↓+2NaOH,该反应属于复分解反应;G和H的反应是铁和氯化铜反应生成氯化亚铁和铜,化学方程式为:Fe+CuCl2=FeCl2+Cu,该反应属于置换反应,反应现象为:铁的表面有红色固体附着,溶液由蓝色变成浅绿色;
(3)通过推导可知,没有涉及到的基本反应类型是分解反应,分解反应是一变多的反应,碳酸钙在高温的条件下生成氧化钙和二氧化碳,化学方程式为:CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑.
故答案为:(1)CaO,Cu(OH)2;
(2)Na2CO3+Ca(OH)2=CaCO3↓+2NaOH,复分解反应;
Fe+CuCl2=FeCl2+Cu,置换反应,铁的表面有红色固体附着,溶液由蓝色变成浅绿色;
(3)分解反应,CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑.
点评 在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可.


科目:初中化学 来源: 题型:解答题
| 编号 | 实验内容 | 实验现象 | 实验结论 |
| 1 | 取反应后固体剩余物0.2g 加入5mL6%的H2O2溶液 | 剧烈反应,放热 产生大量气泡 | 生成物中的MnO2 催化分解H2O2 |
| 2 | 取0.2g MnO2 加入5mL6% (H2O2质量分数)的H2O2溶液 | 平稳反应,放热,持续产生气泡 | MnO2 催化 分解H2O2 |
| 3 | 取反应后固体剩余物1.0g,加入足量水,充分溶解,过滤 | 固体完全溶解,滤纸 上无黑色固体残余物 | 固体剩余物中无 MnO2 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 自然界中的水都呈中性 | |
| B. | 水由氢、氧两种元素组成 | |
| C. | 工农业生产需要大量的淡水 | |
| D. | 地球上的总水储量很大,但淡水很少 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
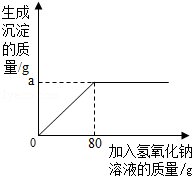 工业上用卤水(主要是MgCl2溶液,另外含少量NaCl)为原料提纯氯化镁;卤水中氯化镁的含量,需通过实验测得.检验员取100g卤水,向里滴加20%的氢氧化钠溶液,所加氢氧化钠溶液质量与所得沉淀的质量关系如图所示.
工业上用卤水(主要是MgCl2溶液,另外含少量NaCl)为原料提纯氯化镁;卤水中氯化镁的含量,需通过实验测得.检验员取100g卤水,向里滴加20%的氢氧化钠溶液,所加氢氧化钠溶液质量与所得沉淀的质量关系如图所示.查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 A、B、C、D、E、F都是初中化学常见的物质,A、C都是维系人类生命最重要的物质,B是用于光合作用和灭火的气体,D可用于保护树木,防止冻伤,并防止害虫生卵,E是人体胃液中含有的酸,它们之间的转化关系如图所示.(“-”表示两端的物质能发生化学反应;“→”表示物质之间的转化关系.)
A、B、C、D、E、F都是初中化学常见的物质,A、C都是维系人类生命最重要的物质,B是用于光合作用和灭火的气体,D可用于保护树木,防止冻伤,并防止害虫生卵,E是人体胃液中含有的酸,它们之间的转化关系如图所示.(“-”表示两端的物质能发生化学反应;“→”表示物质之间的转化关系.)查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com