
【题目】向一定质量FeCl2和CuCl2的混和溶液中逐渐加入足量的锌粒,下列图像所反映得对应关系不正确的是
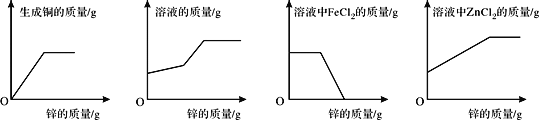
A. A B. B C. C D. D
【答案】D
【解析】由于金属的活动性是锌>铁>铜,向一定质量FeCl2和CuCl2的混和溶液中逐渐加入足量的锌粒,锌先与氯化铜反应,当氯化铜反应完全后再与氯化亚铁反应,反应的方程式是:
Zn+CuCl2=Cu+ZnCl2 溶液增量
65 64 65-64=1
Zn+FeCl2=Fe+ZnCl2 溶液增量
65 56 65-56=9
A、由上述分析可知,锌先与氯化铜反应,生成了铜和氯化锌,铜的质量不断增加,当氯化铜反应完全后不再增加,故A正确;
B、由上述分析可知,锌先与氯化铜反应,当氯化铜反应完全后再与氯化亚铁反应,前者溶液增加的幅度小于后者,故B正确;
C、当锌与氯化铜反应完全后再与氯化亚铁反应,随着锌与氯化亚铁反应,氯化亚铁的逐渐减小,完全反应后质量为0,故C正确;
D、原溶液中不存在氯化锌,起始点应为0,故D错误。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:
【题目】某化学兴趣小组同学用实验室存放近一年的溶质质量分数为30%H202溶液(如下图一),进行如下实验:
(1)小亮从瓶中取出50mL溶液,稀释成10%的H202溶液待用,理论上他需要加水 __ mL。
(2)小丽同学用上述稀释后的H202溶液和下图二装置探究不同物质对H202的催化效果是否相同。实验中她看到左侧试管比右侧试管中产生气泡的速率快,此外还观察到____,说明Mn02对此反应的催化效果比水泥好。请判断该实验设计是否合理并说明理由:____。
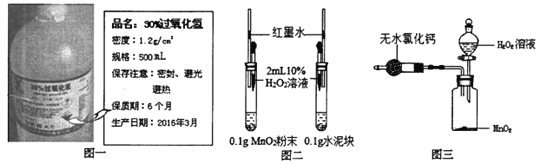
(3)小杰同学用上图三装置测定上述稀释后的H202溶液的溶质质量分数是否为10%,反应前他在分液漏斗中加入50 g稀释后的H202溶液,在干燥管中加入足量无水氯化钙,并在广口瓶中加入适量Mn02样品,共称得装置和药品的总质量力564.57g。打开分液漏斗活塞,使H202溶液全部流入瓶中,迅速关紧活塞,待反应结束后,称得装置及其内所有物质的总质量为562.97g。
①请计算上述稀释后的H202溶液的溶质质量分数与10%是否相符?____(请写出具体计算过程)
②若不符合,其可能的原因是____ 。(注:若符合,此问不作答)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某学生欲称取5.6g氯化钠,他在左边托盘上放了5g砝码,又把游码移到0.6g处,然后在右托盘上加氯化钠直到天平平衡.这时托盘上氯化钠的实际质量是
A.5.6 g B.6.2g C.4.4g D.4.6g
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】清凉油具有散热、醒脑、提神的功效,其主要成分为薄荷脑(化学式为C10H20O),下列有关薄荷脑的说法错误的是
A.薄荷脑是3种元素组成的化合物
B.1个薄荷脑分子中含有31个原子
C.薄荷脑中碳元素的质量分数大于氢元素的质量分数
D.薄荷脑中碳、氢元素的质量比为1:2
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某温度下,在100g质量分数为20%的KNO3 不饱和溶液甲中加入10gKNO3 固体,恰好得到饱和溶液乙,下列说法正确的是
A. 该温度下,KNO3 的溶解度为30g
B. 降低温度,可以使甲溶液变成饱和溶液
C. 乙溶液的质量分数为30%
D. 升高温度,甲、乙两溶液的质量分数都增大
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】Si3N4陶瓷是一种新型无机非金属材料,耐高温,具有较好的机械强度,可以用来制造柴油机。在Si3N4中,N的化合价为-3,则Si的化合价是
A.+1 B.+2 C.+3 D.+4
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲、乙、丙三种固体物质的溶解度曲线如图所示。请回答:
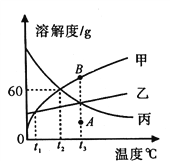
(1)0℃时,三种物质中溶解度最大的是________。
(2)t2℃时,在盛有50g水的烧杯中加入35g甲物质,充分搅拌后所得溶液的质量是_______g。
(3)将t3℃的甲、乙、丙三种物质的饱和溶液降温到t1℃时,所得溶液中溶质的质量分数关系为____________________(用“=”“<”或“>”符号连接)。
(4)将甲溶液由A点转变为B点,可采用的方法是_______(填一种即可)。
(5)如图,将放有固体X的试管放入烧杯中,然后向试管内加入液体Y,一段时间后丙溶液中有固体析出,则对应的X和Y物质是__________(填序号)。
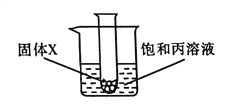
A.氯化钠和水
B.镁条和稀盐酸
C.硝酸铵和水
D.氢氧化钠和水
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列实验操作正确的是( )
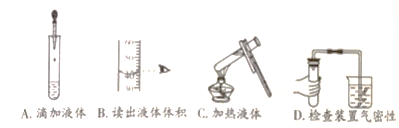
A. 根据使用胶头滴管滴加少量液体的方法进行分析判断
B. 根据量筒读数时视线要与凹液面的最低处保持水平进行分析判断
C. 根据给试管中的液体加热的方法进行分析判断
D. 根据检查装置气密性的方法进行分析判断
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com